
por CenterLab | mar 3, 2022 | Informativos
Dado mais que dobrou em relação ao boletim anterior. Estatística soma os diagnósticos suspeitos aos confirmados.
A Secretaria de Estado de Saúde (SES) divulgou novo boletim da dengue na última terça-feira (28) e mais uma vez os números da doença aumentaram significativamente em Minas Gerais na comparação com o levantamento anterior. Os casos prováveis, por exemplo, mais que dobraram e sofreram um salto de 2.246 para 4.671 – o que dá uma média de 180 diagnósticos suspeitos e confirmados por dia nos 853 municípios.
As mortes investigadas também aumentaram de três para quatro, devido a uma nova suspeita em Iturama, no Triângulo mineiro. As outras três mortes pela dengue ainda investigadas em Minas Gerais neste ano estão distribuídas em Medina (Vale do Jequitinhonha), Além Paraíba (Zona da Mata) e Campo Belo (Centro-Oeste).
Vale lembrar que nem todos os diagnósticos prováveis e mortes sob suspeição aconteceram no período de sete dias, mas sim que eles passaram a fazer parte do levantamento nesse intervalo de tempo.
Ao mesmo tempo, 11 cidades tem incidência muito alta da doença, isto é, mais de 500 casos por 100 mil habitantes. Dessas, apenas Campo Belo, no Centro-Oeste mineiro, não estava na lista da semana passada.
As outras são em incidência muito alta são Josenópolis (Norte), Bandeira (Vale do Jequitinhonha), Inhaúma (Central), Tocantins (Zona da Mata), São Pedro dos Ferros (Zona da Mata), São José da Varginha (Central), Tumiritinga (Vale do Rio Doce), Rodeiro (Zona da Mata), Pingo d’Água (Vale do Rio Doce) e Leme do Prado (Vale do Jequitinhonha).
Há, ainda, três cidades com incidência alta, 23 em média, 272 em baixa e 544 sem registro de caso provável.
Quadros graves e alarmantes
Outra informação trazida pelo levantamento da Saúde estadual diz respeito aos casos de dengue classificados como graves e como alarmantes em Minas Gerais.
Turmalina e Medina, ambas no Vale do Jequitinhonha, e Iturama, no Triângulo, abrigam os três pacientes com quadros clínicos graves.
Enquanto isso, sintomas alarmantes aparecem em 14 moradores do estado. Cinco deles, inclusive, vivem na Grande BH: quatro na capital mineira e outro em Nova Lima. Uberlândia e Uberaba, no Triângulo mineiro, são outras grandes cidades moradores nesta situação – dois e um, respectivamente.
No ano passado, Minas Gerais enfrentou uma epidemia da doença transmitida pelo Aedes aegypti. Foram 482.556 casos, o que deu mais de 50 diagnósticos por hora no estado – a segunda maior quantidade da década, perdendo apenas para 2016. Quanto aos óbitos, em 2019 foram confirmados 173 e 98 permanecem em investigação.
”Salto” na febre chikungunya
O aumento substancial de casos prováveis não fica restrito à dengue. Na semana passada, a Saúde estadual informou que 44 pessoas tinham casos prováveis da febre chikungunya, também transmitida pelo mosquito Aedes aegypti. No levantamento desta semana, o quadro subiu para 82, sendo um em gestante. Não houve mortes.
Outra enfermidade ligada ao inseto é o zika vírus. E, novamente, salto nos casos prováveis, que saíram de 11 para 34. São, até o momento, 11 casos prováveis da doença em Minas Gerais, sendo três em gestantes. No ano passado, foram 702.
Fonte: Eco Diagnóstica

por CenterLab | fev 12, 2022 | Informativos
Desde a Grécia Antiga, há mais de 2.000 anos, foi observada a relação entre a sedimentação das células vermelhas e o fibrinogênio. Para os gregos, a taxa de sedimentação eritrocitária era uma maneira de detectar certos “maus humores orgânicos”. Posteriormente, no início deste século, o teste da velocidade de sedimentação das hemácias (VHS) foi idealizado para auxiliar no diagnóstico da gravidez, sendo posteriormente empregado como indicador de doenças inflamatórias ou infecciosas e até mesmo da condição geral de saúde ou doença.
A padronização desta técnica foi feita em 1920 por Westergren, considerada como padrão-ouro, e foi recomendada pelo Internacional Comitee for Standardization in Hematology de 1973 e referenciado no último conselho internacional de padronização em Hematologia em 1993.
A metodologia proposta por Westergren consiste em colocar o sangue venoso anticoagulado com citrato de sódio a 3,8% (relação 4:1) em um tubo de vidro graduado, 200 mm de comprimento e 2,5mm de diâmetro interno. O tubo é preenchido até a marca zero e deixado na posição vertical por uma hora. A VHS expressa em mm/h será à distância do menisco até o topo da coluna de eritrócitos.
Vários interferentes podem afetar o resultado da VHS como a quantidade e o tipo de anticoagulante usado, produzindo tanto resultados falsamente elevados como falsamente diminuídos, levando à dificuldade interpretativa deste exame. A fundamentação do procedimento se baseia no fato de que a sedimentação eritrocitária depende da agregação das hemácias e da formação de rouleaux. Os eritrócitos possuem carga eletronegativa, por isso repelem-se uns aosoutros, impedindo, durante certo tempo, a agregação e a queda consequente do agregado. Várias proteínas de fase aguda se encontram suspensas no plasma, construindo os coloides eletropositivos, sobretudo o fibrinogênio e globulinas. O aumento da concentração dessas frações proteicas neutraliza as cargas elétricas das membranas dos eritrócitos, rompendo o equilíbrio e assim o agregado globular se deposita. Por esta razão o fenômeno, da formação dos agregados globulares, ocorre paralelamente ao da eritrossedimentação e todas as causas que favorecem, auxiliam igualmente o outro. Baseando-se em tais fatos presume-se que qualquer componente do plasma que afete direta ou indiretamente o grau de agregação dos eritrócitos altera a VHS.
Pode-se citar, por exemplo, que a resposta inflamatória ao dano tecidual inclui alterações na concentração de proteínas plasmáticas, especialmente aumento de fibrinogênio proteína amiloide (SAA) e proteína C-reativa (PCR) e baixa da albumina. Essas alterações ocorrem em inflamações agudas, fases ativas de inflamações crônicas e como consequência de trauma espera-se, nesta situação, um aumento da VHS. É útil na avaliação da resposta ao tratamento de doenças como artrite temporal, polimialgia reumática, febre reumática, artrite reumatoide, Lúpus Eritematoso Sistêmico, tuberculose e endocardite. Entretanto, a presença de VHS normal não exclui doença ativa.
Em processos agudos, pode levar dias para ter valores elevados e estes permanecem por algumas semanas após resolução. Os valores normais aumentam com a idade e inúmeros outros fatores, como gravidez e anemias.Elevações leves a moderadas devem ser interpretadas com cautela nestas situações. Valores muito elevados podem serencontrados em indivíduos com neoplasia maligna, linfoma, carcinoma de colo e mama, doenças hematológicas, doenças do colágeno, doenças renais, infecções graves, cirrose, artrite de grandes células ou polimialgia reumática.
Valores de referência
Os valores de referência da VHS, de acordo com sexo e idade, atualmente utilizados estão listados na Tabela 1.
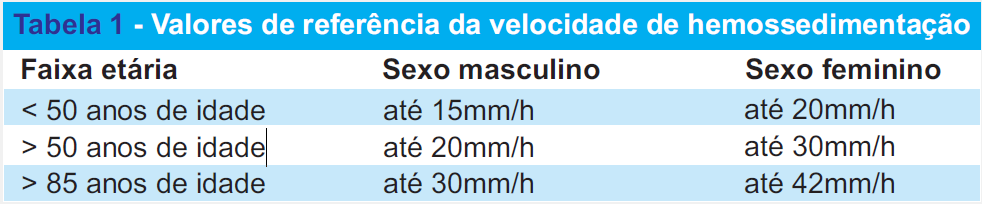
Fatores que influenciam a VHS
Na Tabela 2 estão relacionados fatores capazes de influenciar a VHS. Alguns erros analíticos podem acelerar aVHS levando a resultados falso-positivos. A inclinação do tubo provoca uma separação do plasma e das hemácias, o que promove a formação de rouleaux e aumento da sedimentação. Uma inclinação de apenas 3º pode provocar aumento de até 30% na VHS. Outros fatores, como uma concentração de anticoagulante maior que a recomendada e temperatura ambiente elevada (>25ºC), também aumentam a VHS. O uso de medicamentos, especialmente heparina e contraceptivos orais, é, também, capaz de aumentar a VHS.
Os valores da VHS são mais altos no sexo feminino, o que pode ser explicado, em parte, pelos valores de hematócrito mais baixos nas mulheres e por diferenças hormonais. Há um aumento de VHS de cerca de 0,85mm/h a cada cinco anos de acréscimo na idade. Esta elevação pode estar relacionada ao aumento do fibrinogênio com o avançar da idade. Por outro lado pode ser decorrente da maior prevalência de doenças ocultas em pacientes idosos. Por este motivo, alguns autores recomendam que não se devem utilizar valores de referência maiores para esta faixa etária.
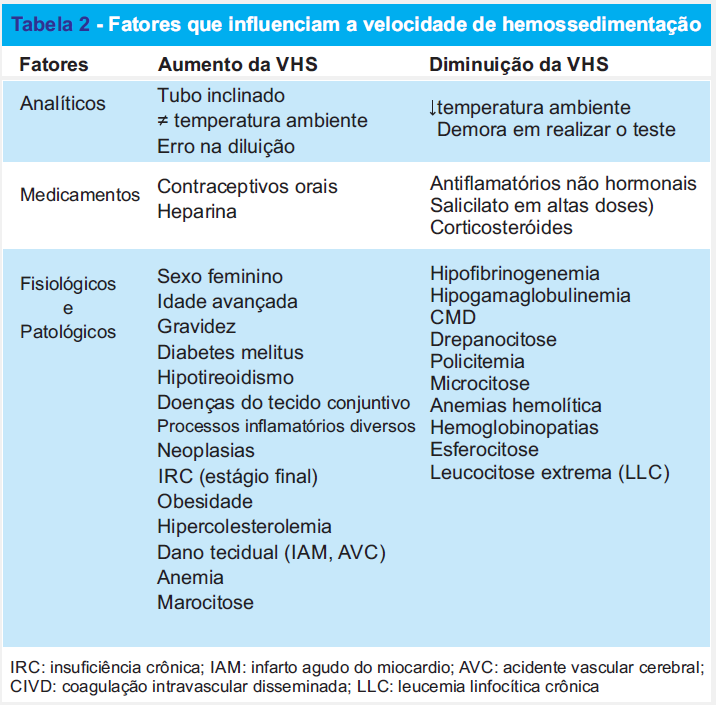
O aumento da VHS na gravidez parece estar relacionado ao aumento do fibrinogênio e à maior prevalência de anemia durante este período. Recentemente, foram sugeridos valores de referência para a VHS em grávidas saudáveis de acordo com o período gestacional e a presença, ou não, de anemia (Tabela 3).

Dentre as condições que aumentam a VHS estão processos de diferentes causas, como doenças malignas, infecções de qualquer natureza, doenças inflamatórias, e várias outras listadas na Tabela 2. A grande variedade de doenças que alteram a VHS em diferentes níveis demonstra o quanto este exame é inespecífico. Na anemia, a sedimentação das hemácias fica facilitada pela redução do número de hemácias em relação ao volume de plasma. Desta forma, em condições associadas à anemia moderada ou grave, a VHS apresenta utilidade bastante limitada.
Vários fatores são capazes de diminuir a VHS (Tabela 2). Dentre os erros analíticos que podem reduzir a VHS levando a resultados falso-negativos, destacam-se a temperatura ambiente mais baixa que a recomendada (<20ºC) e o atraso na realização do teste. O uso de medicamentos como antiinflamatórios não hormonais em altas doses e corticosteróides também diminui a VHS. Este fato tem maior relevância quando o teste é utilizado para verificar a atividade de doenças inflamatórias do tecido conjuntivo, nas quais estes medicamentos são usados com freqüência. O aumento do hematócrito, como na policitemia, dificulta a sedimentação das hemácias. A presença de hemácias falciformes, na drepanocitose, impede a formação de rouleaux. Em ambos os casos, a VHS estará diminuída. A hipofibrinogenemia hereditária primária e a coagulação intravascular disseminada estão entre as enfermidades que reduzem a VHS devido à redução do fibrinogênio. No entanto, valores baixos de VHS apresentam pouco ou nenhum valor diagnóstico.
A Centerlab comercializa o Sistema VSG Aberto Vacuette:
O sistema consiste em tubos VSG (velocidade de sedimentação globular) contém uma solução tamponada de citrato trissódico 3,2% (0.109 mol/L), na proporção de 1 parte de solução de citrato para 4 partes de sangue; Pipeta graduada com adaptador de borracha e Estante VSG sem escala.
Portanto a metodologia utilizada pela Greiner é a Westergren (tradicional), a qual foi padronizada há muitos anos e possui valores de referência específicos.
Referências:
– MERISIO,P.R.; ALFF, F. A. Comparativo das técnicas do exame de velocidade de hemossedimentação (VHS) descrita por Westergren com citrato e a usual com EDTA, NewsLab, ed 120, p. 76-81, 2013. BUCK, A.; VELASQUEZ, P. G.; DÜSMAN, E. Análise comparativa das diferentes diluições para avaliação da velocidade de hemossedimentação-vhs. Arq. Ciênc. Saúde UNIPAR, Umuarama, v. 15, n. 3, p. 213-218, set./dez. 201
– HACHEM, R. H. et al. Velocidade de hemossedimentação (VHS) sem diluição: metodologia confiável? Visão Acadêmica, Curitiba, v.11, n.2, Jul. – Dez./2010.
– COLLARES,G.B.; VIDIGAL,P.G. Recomendações para o uso da velocidade de hemossedimentação. Rev Med Minas Gerais 2004;14(1):52-7.
– Instruções de uso Tubos de VSG para coleta de sangue Vacuette – Greiner bio-one.

por CenterLab | fev 11, 2022 | Informativos
Parâmetros para diferenciação da anemia ferropriva
e talassemia em casos de anemia microcítica
O diagnóstico diferencial das anemias microcíticas é complexo e a sua investigação laboratorial tem um custo. O uso de índices para racionalizar a abordagem diagnóstica tem sido proposto para contornar essa problemática.
Para auxiliar na identificação da causa da anemia microcítica, foi descrito em 1973 por William C. Mentzer, o Índice de Mentzer, sendo útil na diferenciação da anemia ferropriva de beta-talassemia. O índice é gerado a partir dos resultados de um hemograma, sendo utilizados os parâmetros:
– VCM – Volume corpuscular médio (em fL);
– RBC – Contagem global de eritrócitos (RBC, em milhões por microlitro).
Existe um valor de corte para o Índice de Mentzer, sendo que valores abaixo destes são sugestivos para beta talassemia e acima anemia ferropriva. Para entender a utilização deste índice o princípio é o seguinte:
Na deficiência de ferro, a produção de eritrócitos na medula está diminuída. Estes eritrócitos por sua vez são pequenos (microcíticos), de modo que a contagem de ambos parâmetros serão baixos e como resultado, o índice será maior do que o valor de corte. Por outro lado, nos casos de talassemias, a anemia microcítica é resultante de um erro na síntese de cadeias globínicas com consequente diminuição da hemoglobina, sendo a produção dos eritrócitos em quantidade normal mas são mais frágeis e menores com volume corpuscular médio baixo (microcítica), de modo que o índice será menor que o valor de corte.
Além do Índice de Mentzer, o equipamento Celltac G (MEK-9100) da Nihon Kohden tem um parâmetro adicional, o RDWI. Este parâmetro é utilizado em conjunto com o Índice de Mentzer e aumenta significativamente a sensibilidade e especificidade na diferenciação da anemia ferropriva e beta talassemia e consequentemente o diagnóstico final.

Estes índices são muito úteis na orientação ao médico e sem custo adicional. Dessa forma, direciona ao melhor diagnóstico e a melhor tratativa por parte da equipe médica.
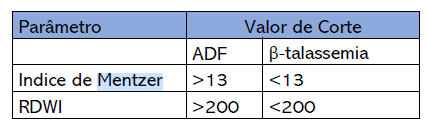 Valor de corte dos Índices referenciados
Valor de corte dos Índices referenciados
Análise de Talassemias Com Celltac ES
Talassemia, também denominada como Anemia do Mediterrâneo devido a maioria dos casos descobertos inicialmente serem habitantes próximos ao Mar do Mediterrâneo, é um tipo de hemoglobinopatia quantitativa, hereditária, decorrentes de mutações nos genes das globinas que promovem redução ou ausência de síntese de uma ou mais das cadeias de globina, formadoras da hemoglobina. O resultado dessas alterações moleculares ocasiona desequilíbrio na produção das cadeias tendo como maior consequência a eritropoese ineficaz.
A Talassemia é classificada como anemia hipocrômica microcítica, tendo essa característica muito similar à anemia ferropriva, sendo que esta última é um estado, no qual há redução da quantidade total de ferro corporal e o fornecimento de ferro é insuficiente para atingir as necessidades de diferentes tecidos, incluindo, principalmente, as necessidades para a formação de hemoglobina e dos glóbulos vermelhos.
Devido a essa similaridade, especialmente no hemograma, há a necessidade de uma rápida identificação diagnóstica, pois isso auxiliará o médico no melhor manejo do paciente. Assim como todos os analisadores hematológicos da Nihon Kohden, o Celltac ES (MEK-7300) possui o parâmetro RDW-SD, um parâmetro eficaz que aliado ao uso de duas agulhas distribui a amostra em suas respectivas câmaras, reduzindo o arraste – Carry Over-, e tornando seus resultados mais precisos. Verificamos a eficácia do parâmetro RDW-SD do Celltac ES (MEK-7300) como um parâmetro potencial para identificação de anemia, comparando contagens de células sanguíneas relacionadas com RBC e histogramas para talassemia e anemia ferropriva. Então, encontramos diferença significativa no RDW-SD de pacientes com talassemia e anemia ferropriva enquanto o RDW-CV e histogramas não mostram diferenças significativas.

Para o rastreio de talassemia, o RDW-SD do Celltac ES (MEK-7300) efetivamente fornece dados eficazes para um diagnóstico preciso do médico, como mostrado na imagem:
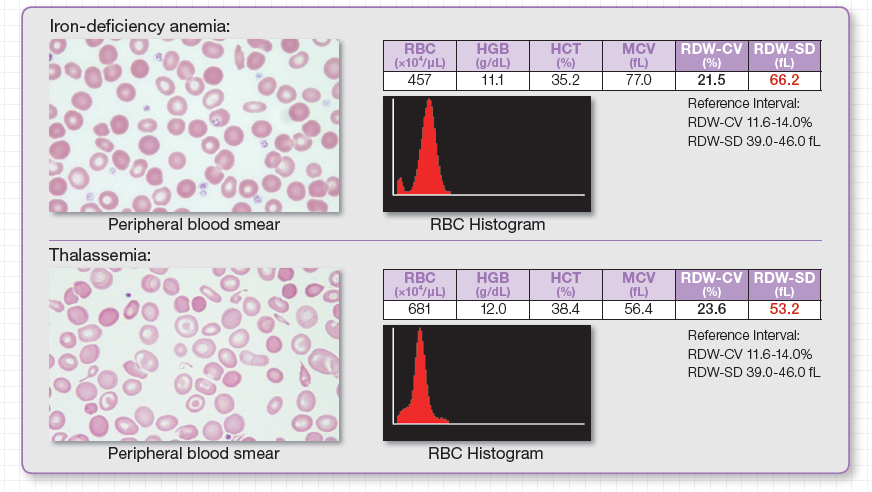
Observa-se a diferença dos histogramas relacionado ao valor do RDW-SD para as diferenciações das duas anemias.
Referências:
– https://www.nihonkohden.com/
– https://br.nihonkohden.com/pt-br/innovativetechnologies/dynascatter_laser/three_new_improvements_in_dynascatter_laser.html
– https://br.nihonkohden.com/pt-br/products/invitrodiagnostics/invitrodiagnostics/automatedbloodcellcounters/mek7300.html

por CenterLab | jan 5, 2022 | Informativos
Infecções sexualmente transmissíveis são problemas de saúde pública no mundo
Depois do surto de peste bubônica, episódio conhecido como Peste Negra, que matou um a cada três habitantes do continente europeu entre os anos de 1347 e 1351, o aparecimento de casos de uma nova e misteriosa doença, em 1495, durante a invasão de Nápoles pelas tropas do rei francês Carlos VIII, gerou um nível de preocupação e medo similar ao experimentado no século XX, quando foi descoberto o HIV.
A Europa estava em franco processo de desenvolvimento e a mudança de hábitos – inclusive sexuais – gerou consequências, já que a transmissão era por meio do ato sexual e velocidade de contaminação espantosa. Em pouco tempo, o “mal”, que recebeu o nome de sífilis, espalhou-se pelos países e passou a “habitar” bordéis, castelos e até monastérios.
Nesse contexto, a bactéria causadora – Treponema pallidum – só foi identificada em 1905 e o primeiro tratamento efetivo foi descoberto em 1910. A cura, por sua vez, só veio em 1945 com a penicilina.
IST
No aparecimento da sífilis, a doença foi chamada de venérea pela forma de contato. O nome dado por um médico francês é uma referência à deusa romana do amor Vênus. No século XX, esse conjunto de problemas de saúde foi chamado de Doenças Sexualmente Transmissíveis (DST) e, no Brasil, atualmente, são as Infecções Sexualmente Transmissíveis (IST). Independentemente do nome, até hoje, elas são um problema de saúde pública de âmbito mundial e também no Brasil, onde o comportamento de risco aumentou o número pessoas infectadas em 2018.
Sabe-se que, além de bactérias, esses males também são causados por vírus e outros microrganismos e que, da sífilis, a lista de tipos aumentou consideravelmente desde a primeira referência, no século XV, e nos dias de hoje inclui herpes genital, gonorreia, tricomoníase, infecção pelo HIV, infecção pelo Papilomavírus Humano (HPV), hepatites virais B e C, infecção pelo vírus linfotrópico de células T humanas (HTLV).
O que não mudou nessa história toda foi a forma de contágio: pelo contato sexual (oral, vaginal e anal) sem uso de camisinha masculina ou feminina, por meio de uma pessoa infectada. A transmissão também pode ocorrer de forma vertical para a criança durante a gestação, no parto ou durante o período de amamentação quando medidas de prevenção previstas não são realizadas.
Além da prevenção, o que pressupõe a mudança de conduta sexual no que se refere ao uso de preservativos e a uma maior atenção a procedimentos como o exame do pré-natal, apenas o diagnóstico e o tratamento efetivo podem melhorar a qualidade de vida do paciente, interromper a cadeia de transmissão e evitar problemas de impacto coletivo, como aumento dos índices de infertilidade, complicações durante a gravidez e o parto e a contaminação congênita de mãe/pai para filho.
No Brasil, as bases para prevenção, diagnóstico e tratamento das IST`s estão bem estabelecidas. O modelo de vigilância epidemiológica é composto por notificação compulsória, serviços sentinela e estudos transversais em determinados grupos populacionais. Além da AIDS, provocada pelo vírus HIV, também são acompanhados os casos de HIV em gestantes, hepatites virais, sífilis em gestantes e adquirida e, ainda, síndrome do corrimento uretral masculino. Em todo território nacional, a notificação compulsória da sífilis congênita, da sífilis em gestantes e da sífilis adquirida teve início em 1986, 2005 e 2010, respectivamente.
Diagnóstico de IST
Cada IST tem o seu sintoma específico. De forma geral, essas infecções se manifestam por meio de feridas, corrimentos e verrugas anogenitais que podem ser acompanhadas por dor pélvica, ardência ao urinar, lesões de pele e aparecimento ou aumento de ínguas. Predominantemente, os sinais característicos aparecem no órgão sexual (masculino ou feminino), mas podem se manifestar em outras partes do corpo também, como palma das mãos, olhos e língua.
Para identificar uma IST no estágio inicial é preciso que o indivíduo observe o próprio corpo durante a higiene pessoal. Quando houver alterações, é recomendado procurar o serviço de saúde, independentemente de quanto tenha ocorrido a última relação sexual e, quando indicado, avisar a parceria para que também procure atendimento médico.
Fonte: Celer
por CenterLab | jan 4, 2022 | Informativos
Microbiologia de Alimento: Doenças Transmitidas por Alimentos (DTAs)
A microbiologia de alimentos é uma área da microbiologia que estuda a interação entre os microrganismos e os produtos alimentícios. Essa interação pode ser benéfica, quando a ação dos microrganismos sobre o alimento o transforma em um novo produto, muitas vezes, deixando-o com mais sabor e/ou maior poder nutricional. No entanto, essa relação também pode ser negativa, onde os microrganismos presentes no alimento apresentam uma ameaça para o consumo seguro do produto.
Um alimento seguro é aquele que não contém agentes ou substâncias nocivas em quantidades que possam causar agravos à saúde ou dano ao consumidor. Esses agentes e substâncias são conhecidos como perigos ou contaminantes (de origem biológica, química ou física) e podem ser prevenidos ou reduzidos por meio de cuidados e regras a serem adotadas durante todas as etapas do preparo e manipulação dos alimentos.
Perigos biológicos são microrganismos vivos que estão presentes nos alimentos e podem causar doenças. Dentre esses, bactérias, vírus, fungos e alguns parasitas que, na maioria das vezes, não podemos ver a olho nu e são as principais causas de doenças transmitidas por alimentos (DTAs).
Doenças Transmitidas por Alimentos (DTAs)
São causadas pela ingestão de alimentos ou água contaminados por microrganismos patogênicos, substâncias químicas ou por toxinas.
Segundo o órgão de saúde americano CDC, há mais de 250 tipos de DTA. No Brasil, segundo a Anvisa, o perfil epidemiológico das DTAs não é bem conhecido, muito pela deficiência dos órgãos de vigilância e a falta de dados médicos.
A manifestação de uma DTA pode ocorrer em uma das seguintes formas:
- Toxinfecção, resulta da ingestão de alimentos contaminados com microrganismos patogênicos que produzem ou liberam toxinas após ingeridos.
- Infecção, decorrente da ingestão e posterior multiplicação do patógeno no intestino, com invasão da mucosa ou penetração de tecidos.
- Intoxicação, causada pela ingestão de toxinas microbianas produzidas durante sua proliferação nos alimentos.
As bactérias constituem o grupo microbiano com a maior incidência nas DTAs, pois apresentam ampla diversidade e virulência, o que lhes confere grande importância frente à sua capacidade de provocar danos à saúde.
As boas práticas são procedimentos que devem ser adotados por indústrias e serviços de alimentação para garantir a qualidade higiênico-sanitária, prevenindo a ocorrência de tais doenças.
No Brasil, desde 2004 essas regras estão definidas por regulamentos federais, a RDC 216 e RDC 331, e a IN 60 da Anvisa.
Microbiologia de alimentos
A microbiologia dos alimentos é uma ciência responsável por estudar a relação dos microrganismos com os alimentos. Por isso, é de extrema importância, já que possibilitou a existência de uma série de processos importantes pelos quais os alimentos passam hoje, que dentre outros fatores, ajudam a evitar doenças e outros fatores patológicos.
Estuda como esses microrganismos podem influenciar as características de produtos alimentícios para consumo humano ou animal, além de estudar os processos causados por eles. Também considerada a ciência dos alimentos, ela ainda engloba aspectos da biotecnologia para a produção e da ecologia microbiana.
As influências de microrganismos podem ser tanto benéficas, quanto prejudiciais. Alguns podem contaminar o alimento e causar doenças em seus hospedeiros, enquanto outros são importantes na produção de alimentos e bebidas, como a levedura na cerveja, por exemplo.
Microrganismos de Interesse em Alimentos
As bactérias, fungos e vírus são os grupos de microrganismos responsáveis por contaminar e causar transformações nos alimentos.
Todo alimento tem uma composição complexa, com grande número de componentes, como água, lipídios, carboidratos, proteínas, vitaminas, sais minerais e ácidos nucléicos, por exemplo. Por isso, as configuram como locais ideais para a habitação e proliferação desses microrganismos.
AGENTES DE DETERIORAÇÃO DOS ALIMENTOS (DETERIORANTES)
O alimento deteriorado teve influência de microrganismos deteriorantes, físicos ou químicos e, por isso, tornou-se impróprio para o consumo humano ou animal. A deterioração pode ser observada por alterações de odor, cor, aspecto, sabor e textura no alimento. Os agentes deteriorantes podem ser fungos, bactérias e leveduras.
AGENTES CAUSADORES DE DOENÇAS (PATOGÊNICOS)
Outra classificação é dos microrganismos como agentes patogênicos que causam as DTAs. Esses microrganismos chegam aos alimentos por meio de diversas vias que, na maioria dos casos, representam condições precárias de higiene em sua produção, distribuição, armazenamento ou manuseio, envolvendo o nível industrial, comercial e doméstico. O tipo de doença e suas características vai depender de fatores como o tipo de microrganismo, o alimento e o indivíduo que o consumiu.
Agentes produtores de alimentos (transformadores)
O alimento transformado teve influência dos microrganismos benéficos, que são capazes de alterar as características originais e transformá-lo em um novo tipo de alimento.
Eles podem ser mantidos ou introduzidos no alimento durante seu processo de produção. Quando ocorrem de maneira natural, é possível estimular sua multiplicação e crescimento. Um mesmo microrganismo pode causar diferentes reações em diferentes alimentos, sendo capaz, até mesmo, de causar efeitos desejáveis em um, enquanto causa deterioração em outro.
Alguns exemplos de agentes transformadores:
Bactérias:
- fermentação do leite (iogurtes e queijos)
- carnes (salames)
- vegetais (picles)
Leveduras:
- fermento na indústria de panificação
- bebidas (cerveja e vinho)
- suplemento alimentar
Fungos:
- fermentação de diversos queijos
- consumidos diretamente (champignon e shitake)
Leveduras do gênero Saccharomyces: Para bebidas alcoólicas e etanol
Acetobacter sp.: Produção de vinagre
Aspergillus niger: Ácido cítrico, amiloglicosidase
Lactobacillus: Ácido lático, bebidas lácteas
Penicillium chrysogenum: Penicilina G
Propionibacterium: Cianocobalamina (B12)
Xanthomonas campestris: Goma Xantana
Corynebacterium glutami: Glutamato monossódico
Escherichia coli e Bacillus megaterium: Penicilina G Acilase
Fatores de Influência no Desenvolvimento dos Microrganismos
Entre os fatores que alteram o desenvolvimento e multiplicação de microrganismos nos alimentos estão os fatores inerentes ao alimento ou parâmetros intrínsecos, e os fatores inerentes ao ambiente, também chamados de parâmetros extrínsecos.

Iniciativas de Controle do Desenvolvimento de Microrganismos
Antissépticos: produtos antissépticos evitam que tecidos sejam infectados, o que contribui para impedir ou matar os microrganismos. Por serem aplicados em tecidos vivos, geralmente, os antissépticos são menos tóxicos que os desinfetantes (aplicados em materiais inanimados);
Germicidas: os germicidas matam microrganismos, mas não matam endosporos;
Desinfecção: esse processo remove, mata ou inibe microrganismos patogênicos e saprófitas sem eliminar todas as formas de vida presentes;
Esterilização: destrói todas as formas de vida microbiana, incluindo endosporos;
Esterilização Comercial: tratamento de calor suficiente para matar os endósporos do Clostridium botulinum (bactéria patogênica que pode gerar uma toxinfecção alimentar) em alimentos enlatados;
Sanitização: reduz os microrganismos a níveis seguros seguindo os padrões de saúde pública (eliminação de 99,9% das formas vegetativas).
Os estudos da microbiologia de alimentos foram e ainda são indispensáveis para a qualidade da saúde humana e animal. Sem os conhecimentos adquiridos por meio dessa ciência dos alimentos, não seria possível ter a qualidade que temos hoje. Por isso, é um assunto relevante para as pessoas no geral, além de ter extrema importância para indústrias, empresas, lojas e restaurantes em geral do ramo alimentício.

por CenterLab | jan 4, 2022 | Informativos
Qualidade da Água na Indústria Farmacêutica
Na indústria farmacêutica, a qualidade da água adquire algumas funções importantes. Além de participar dos processos de limpeza de materiais e superfícies, é uma das principais matérias-primas que entram na formulação dos produtos, o que exige grande atenção e análise em sua composição. Por ser um solvente universal, a água pode carregar consigo substâncias que comprometem não somente a qualidade dos medicamentos, mas também a vida útil dos sistemas de tratamento.
Os processos farmacêuticos são altamente delicados, o que exige o uso de materiais e equipamentos especializados e substâncias tratadas, inclusive a água, para evitar a degradação da composição química dos medicamentos.
Mesmo sendo considerada própria para o consumo, a água potável ainda possui substâncias que podem comprometer as propriedades das fórmulas dos medicamentos. Para ser utilizada para tal finalidade, a água precisa passar por diversos processos para evitar que impurezas e microrganismos alterem o resultado dos procedimentos.
Água como matéria-prima
A água é a matéria-prima mais utilizada na produção farmacêutica, de biotecnologia, correlatos e cosméticos. Pode ser utilizada direta ou indiretamente, podendo ter grande impacto na qualidade do produto. Os requisitos de qualidade da água dependerão de sua finalidade e emprego, e da escolha do sistema de purificação para atender ao grau de pureza estabelecido.
O processo de purificação da água para uso farmacêutico é baseado na eliminação de impurezas físico-químicas, biológicas e microbianas até se obter níveis preestabelecidos em compêndios oficiais aprovados pelas autoridades sanitárias como a ANVISA e a Farmacopéia Brasileira (FB).
Tipos de água
Existem diferentes tipos de água dentro de uma indústria farmacêutica. Dentre elas, podemos destacar:
Água Potável
O ponto de partida para qualquer processo de purificação de água para fins farmacêuticos é a água potável. É obtida por tratamento da água retirada de mananciais, por meio de processos adequados para atender às especificações da legislação brasileira e deve estar em conformidade com os limites físicos, químicos e microbiológicos. É empregada, normalmente, nas etapas iniciais de procedimentos de limpeza e como fonte de obtenção de água de mais alto grau de pureza. Pode ser utilizada também na climatização térmica de alguns aparatos e na síntese de ingredientes intermediários.
Água Purificada (AP)
É produzida a partir da água potável e não contém qualquer substância adicionada, sendo obtida por combinação de sistemas de purificação em uma sequência lógica, tais como múltipla destilação, troca iônica, osmose reversa, eletrodeionização, ultrafiltração ou outro processo capaz de atender, com a eficiência desejada, aos limites especificados para os diversos contaminantes conforme a FB.
É empregada como excipiente na produção de formas farmacêuticas não parenterais e em formulações magistrais, desde que não haja nenhuma recomendação de pureza superior no seu uso ou que não necessite ser apirogênica. Também, pode ser utilizada na lavagem de material, preparo de soluções reagentes, meios de cultura, tampões, diluições diversas, microbiologia em geral, análises clínicas ou análises qualitativas ou quantitativas menos exigentes (determinações em porcentagem).
Água Ultrapurificada (AUP)
Possui baixa concentração iônica, baixa carga microbiana e baixo nível de carbono orgânico total (COT), sendo requerida em aplicações mais exigentes, principalmente em laboratórios de ensaios para diluição de substâncias de referência e na limpeza final de equipamentos e utensílios utilizados em processos que entrem em contato direto com a amostra. A utilização dessa água é essencial para a obtenção de resultados analíticos precisos. Deve ser utilizada no momento em que é produzida, ou no mesmo dia da coleta.
Água para Injetáveis (API)
Água para injetáveis é utilizada como excipiente na preparação de produtos farmacêuticos parenterais de pequeno e grande volume, na fabricação de princípios ativos de uso parenteral, de produtos estéreis, demais produtos que requeiram o controle de endotoxinas e não são submetidos à etapa posterior de remoção. É utilizada ainda na limpeza e preparação de processos, equipamentos e componentes que entram em contato com fármacos e medicamentos estéreis durante sua produção.

Tipos de contaminantes que impactam na qualidade da água
O controle da contaminação da água é crucial, uma vez que a água tem grande capacidade de agregar compostos diversos e, também, de se contaminar novamente após a purificação. Os contaminantes da água são representados por dois grandes grupos:
Contaminante Químico
Os contaminantes orgânicos e inorgânicos têm origens diversas: da fonte de alimentação, da extração de materiais com os quais a água entra em contato, da absorção de gases da atmosfera, de resíduos poluentes ou resíduos de produtos utilizados na limpeza e sanitização de equipamentos, dentre muitos outros. Incluem-se aqui as endotoxinas bacterianas, resultantes de microrganismos gram-negativos, contaminantes críticos que devem ser removidos adequadamente. Esses contaminantes podem ser avaliados, principalmente, pelos ensaios de carbono orgânico total – COT e de condutividade.
Contaminante Microbiológico
São representados principalmente por bactérias e apresentam um grande desafio à qualidade da água. São originários da própria microbiota da fonte de água e de alguns equipamentos de purificação. Podem surgir, também, devido a procedimentos de limpeza e sanitização inadequados, que possibilitam à formação de biofilmes e, por consequência, instalam um ciclo contínuo de crescimento a partir de compostos orgânicos que, em última análise, são os próprios nutrientes para os microrganismos.
As bactérias podem afetar a qualidade da água por desativar reagentes ou alterar substratos por ação enzimática, aumentar o conteúdo em COT, alterar a linha de base (ruído de fundo) em análises espectrais e produzir pirogênios, como as endotoxinas.
Para garantir a boa qualidade da água na indústria farmacêutica, é preciso estar atento a todas as etapas. Os sistemas de produção, armazenamento e distribuição de água para uso farmacêutico devem ser planejados, instalados, validados e mantidos de forma a garantir a produção de água de qualidade apropriada sempre obedecendo os níveis preestabelecidos em compêndios oficiais aprovados pelas autoridades sanitárias vigentes no país.
Fonte: Kasvi









 Valor de corte dos Índices referenciados
Valor de corte dos Índices referenciados





