
por CenterLab | jan 4, 2022 | Informativos
Qualidade da Água na Indústria Farmacêutica
Na indústria farmacêutica, a qualidade da água adquire algumas funções importantes. Além de participar dos processos de limpeza de materiais e superfícies, é uma das principais matérias-primas que entram na formulação dos produtos, o que exige grande atenção e análise em sua composição. Por ser um solvente universal, a água pode carregar consigo substâncias que comprometem não somente a qualidade dos medicamentos, mas também a vida útil dos sistemas de tratamento.
Os processos farmacêuticos são altamente delicados, o que exige o uso de materiais e equipamentos especializados e substâncias tratadas, inclusive a água, para evitar a degradação da composição química dos medicamentos.
Mesmo sendo considerada própria para o consumo, a água potável ainda possui substâncias que podem comprometer as propriedades das fórmulas dos medicamentos. Para ser utilizada para tal finalidade, a água precisa passar por diversos processos para evitar que impurezas e microrganismos alterem o resultado dos procedimentos.
Água como matéria-prima
A água é a matéria-prima mais utilizada na produção farmacêutica, de biotecnologia, correlatos e cosméticos. Pode ser utilizada direta ou indiretamente, podendo ter grande impacto na qualidade do produto. Os requisitos de qualidade da água dependerão de sua finalidade e emprego, e da escolha do sistema de purificação para atender ao grau de pureza estabelecido.
O processo de purificação da água para uso farmacêutico é baseado na eliminação de impurezas físico-químicas, biológicas e microbianas até se obter níveis preestabelecidos em compêndios oficiais aprovados pelas autoridades sanitárias como a ANVISA e a Farmacopéia Brasileira (FB).
Tipos de água
Existem diferentes tipos de água dentro de uma indústria farmacêutica. Dentre elas, podemos destacar:
Água Potável
O ponto de partida para qualquer processo de purificação de água para fins farmacêuticos é a água potável. É obtida por tratamento da água retirada de mananciais, por meio de processos adequados para atender às especificações da legislação brasileira e deve estar em conformidade com os limites físicos, químicos e microbiológicos. É empregada, normalmente, nas etapas iniciais de procedimentos de limpeza e como fonte de obtenção de água de mais alto grau de pureza. Pode ser utilizada também na climatização térmica de alguns aparatos e na síntese de ingredientes intermediários.
Água Purificada (AP)
É produzida a partir da água potável e não contém qualquer substância adicionada, sendo obtida por combinação de sistemas de purificação em uma sequência lógica, tais como múltipla destilação, troca iônica, osmose reversa, eletrodeionização, ultrafiltração ou outro processo capaz de atender, com a eficiência desejada, aos limites especificados para os diversos contaminantes conforme a FB.
É empregada como excipiente na produção de formas farmacêuticas não parenterais e em formulações magistrais, desde que não haja nenhuma recomendação de pureza superior no seu uso ou que não necessite ser apirogênica. Também, pode ser utilizada na lavagem de material, preparo de soluções reagentes, meios de cultura, tampões, diluições diversas, microbiologia em geral, análises clínicas ou análises qualitativas ou quantitativas menos exigentes (determinações em porcentagem).
Água Ultrapurificada (AUP)
Possui baixa concentração iônica, baixa carga microbiana e baixo nível de carbono orgânico total (COT), sendo requerida em aplicações mais exigentes, principalmente em laboratórios de ensaios para diluição de substâncias de referência e na limpeza final de equipamentos e utensílios utilizados em processos que entrem em contato direto com a amostra. A utilização dessa água é essencial para a obtenção de resultados analíticos precisos. Deve ser utilizada no momento em que é produzida, ou no mesmo dia da coleta.
Água para Injetáveis (API)
Água para injetáveis é utilizada como excipiente na preparação de produtos farmacêuticos parenterais de pequeno e grande volume, na fabricação de princípios ativos de uso parenteral, de produtos estéreis, demais produtos que requeiram o controle de endotoxinas e não são submetidos à etapa posterior de remoção. É utilizada ainda na limpeza e preparação de processos, equipamentos e componentes que entram em contato com fármacos e medicamentos estéreis durante sua produção.

Tipos de contaminantes que impactam na qualidade da água
O controle da contaminação da água é crucial, uma vez que a água tem grande capacidade de agregar compostos diversos e, também, de se contaminar novamente após a purificação. Os contaminantes da água são representados por dois grandes grupos:
Contaminante Químico
Os contaminantes orgânicos e inorgânicos têm origens diversas: da fonte de alimentação, da extração de materiais com os quais a água entra em contato, da absorção de gases da atmosfera, de resíduos poluentes ou resíduos de produtos utilizados na limpeza e sanitização de equipamentos, dentre muitos outros. Incluem-se aqui as endotoxinas bacterianas, resultantes de microrganismos gram-negativos, contaminantes críticos que devem ser removidos adequadamente. Esses contaminantes podem ser avaliados, principalmente, pelos ensaios de carbono orgânico total – COT e de condutividade.
Contaminante Microbiológico
São representados principalmente por bactérias e apresentam um grande desafio à qualidade da água. São originários da própria microbiota da fonte de água e de alguns equipamentos de purificação. Podem surgir, também, devido a procedimentos de limpeza e sanitização inadequados, que possibilitam à formação de biofilmes e, por consequência, instalam um ciclo contínuo de crescimento a partir de compostos orgânicos que, em última análise, são os próprios nutrientes para os microrganismos.
As bactérias podem afetar a qualidade da água por desativar reagentes ou alterar substratos por ação enzimática, aumentar o conteúdo em COT, alterar a linha de base (ruído de fundo) em análises espectrais e produzir pirogênios, como as endotoxinas.
Para garantir a boa qualidade da água na indústria farmacêutica, é preciso estar atento a todas as etapas. Os sistemas de produção, armazenamento e distribuição de água para uso farmacêutico devem ser planejados, instalados, validados e mantidos de forma a garantir a produção de água de qualidade apropriada sempre obedecendo os níveis preestabelecidos em compêndios oficiais aprovados pelas autoridades sanitárias vigentes no país.
Fonte: Kasvi

por CenterLab | out 31, 2020 | Informativos
Uma das principais finalidades dos resultados dos exames laboratoriais é reduzir as dúvidas que a história clínica e o exame físico fazem surgir no raciocínio médico. Para que o laboratório clínico possa atender, adequadamente, a este propósito, é indispensável que todas as fases do atendimento ao paciente sejam desenvolvidas seguindo os mais elevados princípios de correção técnica, considerando a existência e a importância de diversas variáveis biológicas que influenciam, significativamente, a qualidade final do trabalho.
Atualmente cerca de 60 a 70% dos erros laboratoriais estão concentrados na fase pré-analítica em laboratórios clínicos que possuem um sistema de controle de qualidade bem estabelecido, devido a esse número expressivo iremos abordar essa fase neste boletim, lembrando que existem as fases Analítica e Pós-Analitica.
Fase Pré Analítica
A fase pré-analítica inclui a indicação do exame, redação da solicitação de eventuais instruções de preparo do paciente, avaliação do atendimento às condições prévias, procedimento de coleta, acondicionamento, preservação e transporte da amostra biológica até o momento em que o exame seja, efetivamente, realizado.
Para a coleta de sangue e realização de exames laboratoriais, é importante que se conheça, controle e, se possível, evite algumas variáveis que possam interferir na exatidão dos resultados. Classicamente, são referidas como condições pré-analíticas: variação cronobiológica, gênero, idade, posição, atividade física, jejum, dieta e uso de drogas para fins terapêuticos ou não.
Inúmeras variáveis pré-analíticas podem ser responsáveis pelas falhas nesse processo, sendo as mais relevantes:
– amostra insuficiente;
– amostra incorreta;
– amostra inadequada;
– identificação incorreta;
– problemas no acondicionamento e transporte da amostra.
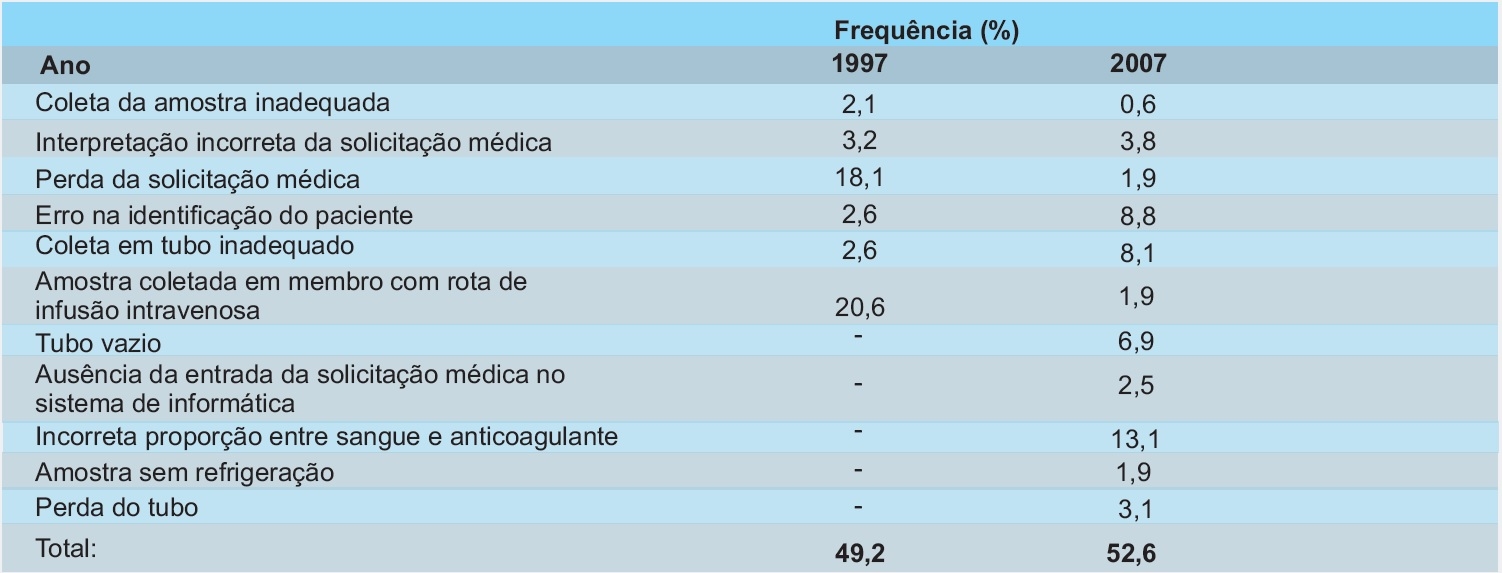
Tabela 1 – Freqüência de erros na fase pré analítica em laboratórios clínicos
Venopunçao
A venopunção é um procedimento complexo, que exige conhecimento e habilidade. Quando uma amostra de sangue for colhida, um profissional experiente deve seguir varias etapas, como: verificar a solicitação medica apresentar-se ao paciente, estabelecer uma comunicação clara com mínimo de termos técnicos possíveis, passar confiança, explicar todo procedimento
obtendo consentimento para o procedimento, realizar a assepsia das mãos entre os pacientes, realizar a identificação do paciente confirmando os dados pessoais e comparando-os ao pedido medico, caso paciente inconsciente realizar comparação com o bracelete de internação e confirmar os dados cadastrais com acompanhante ou equipe da enfermagem assistencial, anotando nome de quem forneceu as informações, paciente semiconscientes, comatosos ou dormindo devem ser despertado antes da coleta, verificar as condições de preparo e o jejum do paciente está adequados e indagar sobre eventuais alergia ao látex.
Para realização da coleta de sangue, alguns aspectos devem ser analisados, como:
– Local de Escolha da Venopunção;
– Uso Adequado do Torniquete;
– Procedimento para Antissepsia e Higienização em Coleta de Sangue Venoso;
– Higienização das mãos;
– Vestir as Luvas;
– Antissepsia do local da punção;
É importante ter a consciência de que as medidas dessas falhas nos diversos processos, por meio de levantamento de indicadores, podem contribuir para busca de causa e consequentemente melhora do processo.
Para uma melhor compressão do assunto e uma leitura mais aprofundada, recomendamos a leitura “Recomendações da Sociedade Brasileira de Patologia Clínica Medicina Laboratorial para Coleta de Sangue Venoso”.
A Centerlab em parceria com a Greiner Bio-one apresenta toda linha de material com a mais alta tecnologia e pensado na Biossegurança de seus colaboradores e pacientes atendendo as normas da NR 32 – Segurança e Saúde no Trabalho em Serviços de Saúde, com diferencias como:
Tubos de Coleta com Trava de Segurança:
Os tubos Vacuette apresentam segurança aos colaboradores, pois evitam os efeitos Detonador e Aerossol.
Detonador: o sangue após a coleta, ao ser depositado dentro do tubo de sangue a vácuo, continua com suas células sanguíneas vivas em plena atividade (metabolismo). Desta forma as células trocam gases aumentando a pressão interna no tubo possibilitando o desprendimento da tampa e expondo a amostra.
Aerossol: são pequenas partículas de sangue que ficam suspensas no ar dentro do tubo de sangue. No momento da abertura do tubo para realizar os exames essas partículas são expelidas para o meio externo e os colaboradores na qual promovem a abertura podem respirar essas amostras expelidas para o micro ambiente promovendo risco aso colaboradores.

Ambos os efeitos acima promovem riscos aos colaboradores, perda de amostra e consequentemente interferência no desempenho da fase pré-analítica. Ambos os efeitos são impedidos quando os tubos de coleta são de rosca propiciando melhor qualidade da amostra e menor exposição da mesma ao ambiente, evitando riscos biológicos para colaboradores em todas as etapas do processo.
Além dos tubos de coleta contamos com toda linha de produtos com a mais alta tecnologia para ajudar neste processo laboratorial, incluindo: Adaptadores de Segurança nos modelos
QuickShield, Holdex, Escalpes com Trava, Agulhas, Agulhas Visio Plus, Anéis de Identificação, tubos para coletas infantil ou de difícil acesso (MiniCollect).
Avanços em Punção Venosa – Escaneamento de Veias
Os profissionais que coletam sangue sabem que o domínio de uma boa técnica de punção venosa é importante, principalmente em determinadas áreas de atuação, tais como Pronto Socorro, Pediatria e UTI. Porém, sabe-se que nem todos os pacientes são/estão “bons de veia”.
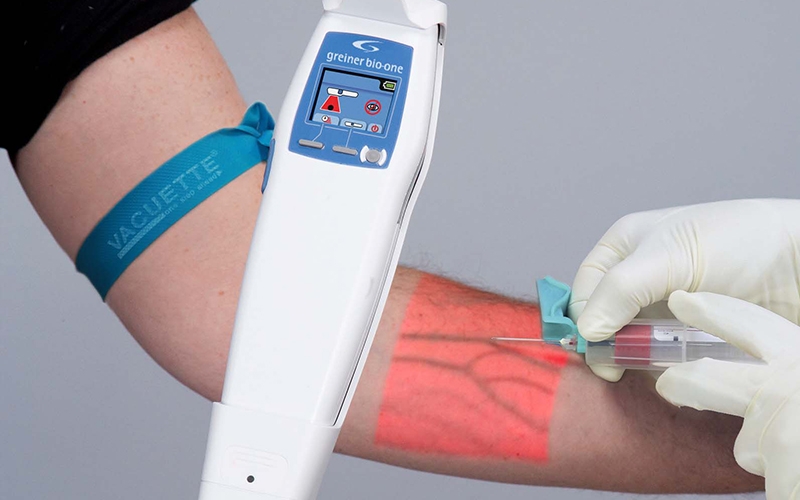
Apesar da alta qualificação dos profissionais em acessos difíceis, muitos ainda enfrentam esse desafio com esse tipo de punção venosa.
Para auxiliar nessas dificuldades podemos lançar mão da tecnologia dos escaneamento das veias através de equipamentos que utiliza tecnologia de raios infravermelhos, os quais são absorvidos pelo sangue subcutâneo, permitindo assim que se forme um “mapa” das veias, permitindo a localização de válvulas e bifurcações em tempo real durante o procedimento auxiliando na punção venosa, além disso, é possível extravasamento de sangue no tecido cutâneo, evitando assim possível complicações como edemas.
Referencias Bibliográficas:
– https://www.gbo.com/pt_BR.html
– Recomendações da Sociedade Brasileira de Patologia Clínica Medicina Laboratorial para Coleta de Sangue Venoso.
– https://controllab.com/pdf/livro_sbpc_interferentes_2018.pdf
-http://www.sbpc.org.br/noticias-e-comunicacao/erros-na-fase-pre-analitica-alteram-resultadoshttps://www.fleury.com.br/medico/artigos-cientificos/exames-laboratoriais-e-a-importancia-dos-cuidados-pre-analiticos

por CenterLab | out 19, 2020 | Informativos
O Controle de Qualidade é um conjunto de práticas utilizadas para monitorar os processos de análise dos exames laboratoriais e tem o objetivo principal de garantir a confiabilidade dos resultados obtidos, através das análises realizadas.
Muito difundido entre os laboratórios de análises clínicas, o Controle de Qualidade é um processo essencial para o funcionamento destes estabelecimentos e deixou de ser apenas uma boa prática, para se tornar uma exigência da Agência Nacional de Vigilância Sanitária (Anvisa), de acordo com a RDC 302/2005. Para os laboratórios e clínicas veterinárias, ainda não se tem uma normativa que verse sobre a obrigatoriedade do Controle de Qualidade. Apesar disto, é uma boa prática os laboratórios e clínicas quanto aos resultados de exames laboratoriais.
A diferença entre Controle de Qualidade Interno e Externo
O processo de Controle de Qualidade contempla duas principais ferramentas complementares: Controle de Qualidade Interno (CQI) e Controle de Qualidade Externo (CQE), também conhecido como Ensaio de Proficiência. “Juntos, eles têm o propósito central de identificar a presença de possíveis erros analíticos, possibilitando ao laboratório a implantação de ações para eliminar as causas dos mesmos”, afirma Jéssica Gomes, do setor de Gestão de Serviços da Controllab.
“O CQI é realizado com a rotina de análise de amostras dos pacientes, para validar os resultados produzidos, após identificar que o sistema analítico está operando dentro dos limites de tolerância predefinidos, especialmente a precisão do processo (reprodutibilidade). O CQE ou Ensaio de Proficiência realiza um acompanhamento das tendências dos processos (inexatidão), comumente relacionadas a características de linearidade, especificidade, sensibilidade, interferentes e calibração”, complementa Jéssica.
Segundo Flávia Mirian, do setor de Gestão de Marketing da Controllab, o Controle de Qualidade em laboratórios veterinários tem grande importância, uma vez que é capaz de gerar informações para o laboratório e proporcionar confiabilidade nos resultados liberados. Flávia ainda ressalta sobre “a necessidade de conscientização dos profissionais responsáveis pelos laboratórios veterinários sobre esta importância e que este é um processo construído e amadurecido ao longo do tempo”.
Um Ensaio de Proficiência específico para a veterinária
Quando um laboratório participa de Ensaios de Proficiência, é possível obter certificação, de acordo com o ano de participação, se o mesmo obtiver resultados satisfatórios ao longo do ano de participação. A Controllab dispõe em seu portfólio de um Ensaio de Proficiência específico para a veterinária.
“O programa teve seu início em 2006 e, desde 2008, conta com a parceria da Sociedade Brasileira de Medicina Veterinária (SBMV)”, aponta Flávia. O programa conta com mais de 10 áreas de atuação, incluindo Bioquímica, Urinálise, Hematologia, entre outros.
De acordo com Flávia, o Ensaio de Proficiência funciona periodicamente. Múltiplos itens em diferentes concentrações são enviados aos laboratórios e clínicas participantes do programa e, normalmente, ocorrem quatro rodadas anuais. O programa é baseado na norma ABNT NBR ISO 17043, mesma normativa dos programas de Proficiência de laboratórios de análises clínicas, cujo provedor é acreditado pela Cgcre/Inmetro (PEP 003). A abrangência é nacional e internacional, contando cerca de 150 participantes, entre laboratórios, clínicas e pets.
Os materiais utilizados no CQE e no CQI são produzidos em variadas concentrações e matrizes, sempre que possível, similar à analisada na rotina, contemplando animais de pequeno a grande porte e suas especificidades, conforme a relevância clínica. Na Medicina Veterinária, os exames laboratoriais são realizados nas mais diferentes espécies: canina, felina, bovina, equina, ovina, suína, entre outras. Por isso, a preocupação de materiais controlados em matrizes específicas que representem esta grande variedade de espécies.
Além disso, Flávia e Jéssica complementam que o Ensaio de Proficiência Veterinário está em constante expansão e novas áreas de atuação poderão ser incluídas, de acordo com a necessidade dos clientes e do mercado.
Controles internos para parâmetros bioquímicos
A Controllab disponibiliza em seu portfólio controles internos para análises bioquímicas veterinárias para múltiplos analitos. Os controles internos são soro canino e equino liofilizados em dois níveis, com apresentação de 2 x 3,0 mL.
É importante se atentar para os valores de referência de cada espécie e para a linearidade e sensibilidade dos métodos utilizados para atribuição de valor dos controles. “A atribuição de valor pode ser realizada por consenso, comparação interlaboratorial ou pelo laboratório de ensaios da Controllab, que é acreditado pela ABNT NBR ISO 17025”, complementa Jéssica.
A Centerlab possuí em seu portifólio de produtos o controle de qualidade interno para análises bioquímicas veterinárias da Labtest, o Qualitrol 1 VET Ref. 1014. É uma preparação liofilizada e possui apresentação de 1 x 5,0 mL. O Qualitrol 1 VET Ref. é um controle multiparamétrico e conta com valores atribuídos para sistemas com leituras mono e bicromáticas, além do sistema de química seca.
Fonte: Labtest

por CenterLab | abr 13, 2019 | Informativos

BrCAST
A Centerlab em parceria com a Laborclin entende que muito além de nossos objetivos comerciais, possuímos a missão e a responsabilidade de compartilhar conhecimento técnico e científico, ajudando a melhor promover a saúde pública no país.
Em 14 de dezembro de 2018, o Ministério da Saúde publicou a Portaria nº 64 de 11/12/2018 que “Determina aos laboratórios de rede pública e rede privada, de todas as Unidades Federadas, a utilização das normas de interpretação para os testes de sensibilidade aos antimicrobianos (TSA), tendo como base os documentos da versão brasileira do European Committee on Antimicrobial Susceptibility Testing, o BrCAST”.
Segundo o documento, a medida foi tomada devido à necessidade de padronização da interpretação dos testes de sensibilidade aos antimicrobianos nos laboratórios clínicos e de pesquisa, assim como fortalecer a rede laboratorial, melhorando a qualidade dos resultados para uma melhor vigilância epidemiológica e clínica. Tais ações ajudariam adequadamente a prescrição de medicamentos, bem como auxiliariam as medidas de prevenção e controle para impedir a disseminação de doenças infecto-contagiosas.
O BrCAST é um comitê designado conjuntamente pela Sociedade Brasileira de Análises Clínicas, Sociedade Brasileira de Infectologia, Sociedade Brasileira de Microbiologia e Sociedade Brasileira de Patologia Clínica e Medicina Laboratorial. Os
objetivos principais são representar o Brasil nas instituições que atuem ativamente na padronização de testes de sensibilidade aos antimicrobianos e buscar um consenso internacional e/ou harmonização com o European Committee on Antimicrobial Susceptibility Testing (EuCAST) e o Clinicas and Laboratory Standart Institute (CLSI).
O Teste de Sensibilidade a Antimicrobianos tem como objetivos ser um guia na escolha da terapia racional, garantir a eficácia microbiana quando a sensibilidade não pode ser prevista, e fornecer dados epidemiológicos.
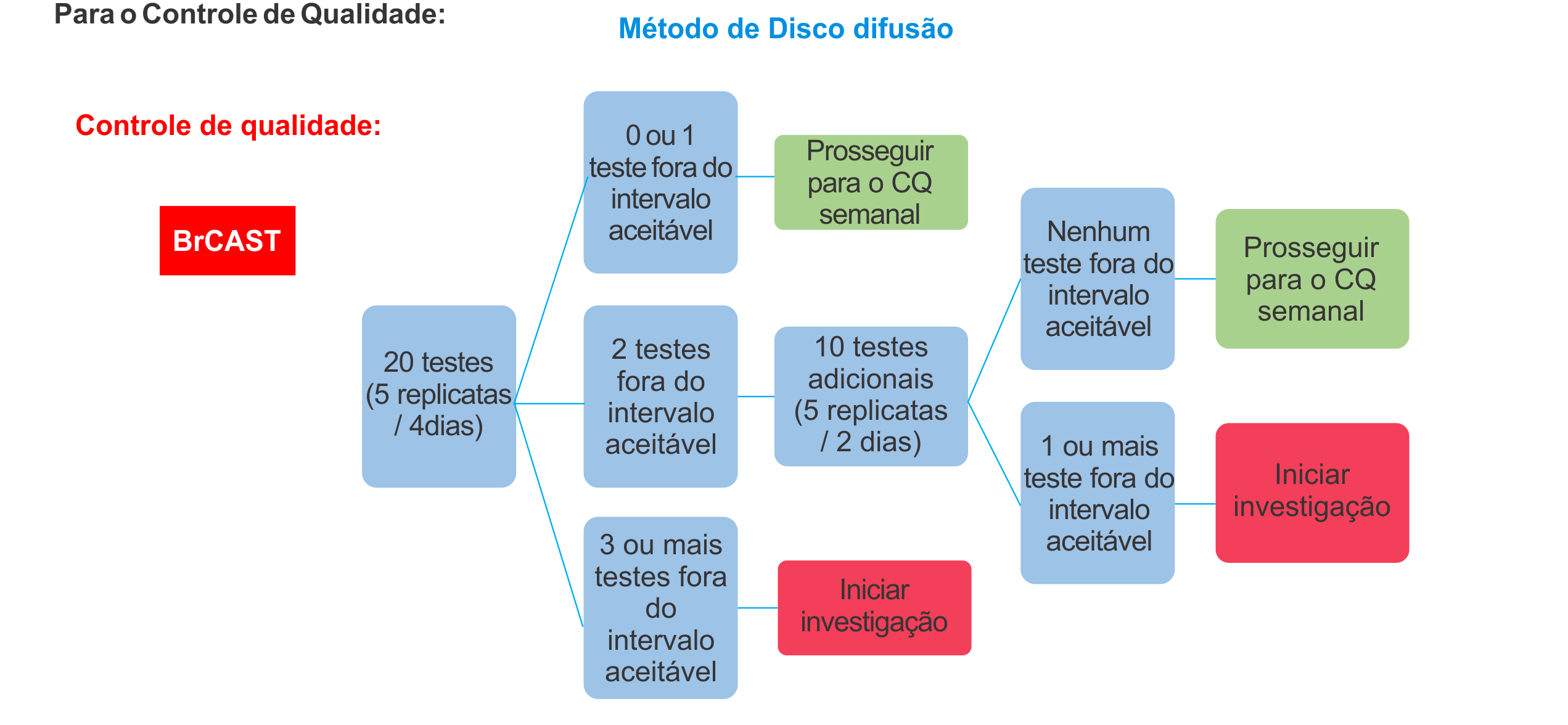
Os documentos do BrCAST disponíveis, gratuitos e em português incluem Tabelas de Pontos de Corte, Tabelas de Controle de Qualidade, Manual de Disco Difusão, Guia de Leitura e Lista para implantação. O prazo para os laboratórios se adequarem à metodologia BrCAST é de 12 meses, contados a partir da data de publicação desta Portaria.
Para iniciar a implantação é necessário:
– identificar o método a ser utilizado (manual , automação, etc);
– encontrar documentos necessários – para isto acessar brcast.org.br;
– conferir os materiais necessários;
– comparar os documentos, BrCAST X CLSI para facilitar adequação.
As principais modificações presentes neste novo padrão de antibiogramas consistem em:
– Alteração do tipo de ágar para a leitura do TSA em microrganismos fastidiosos. O CLSI indica a utilização do ágar Mueller
Hinton com 5% de sangue de carneiro, já o BrCAST padroniza a utilização de Mueller Hinton com 5% de sangue de cavalo e
20mg/L β-NAD.
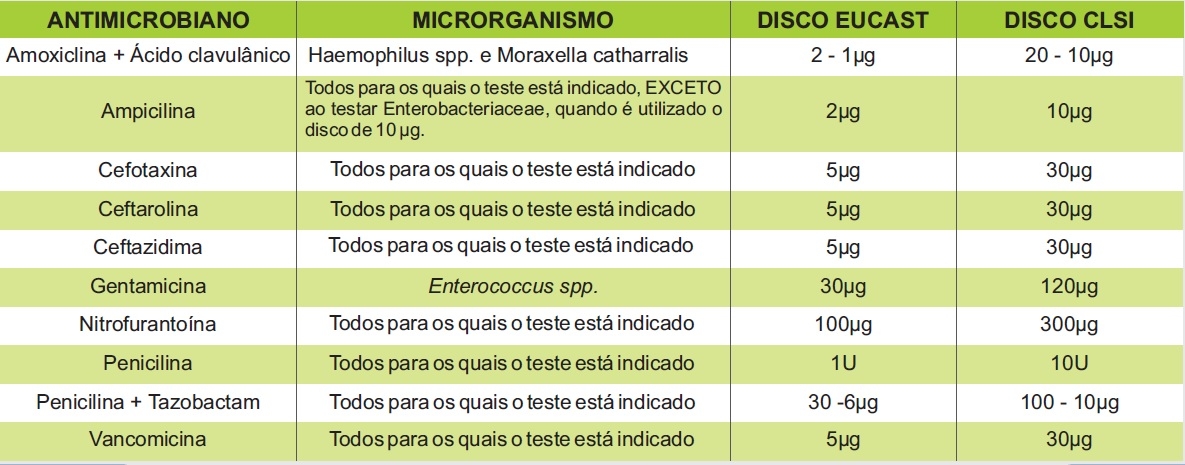
– Alteração da concentração de dez antibióticos utilizados, como mostra a tabela abaixo.
– Incubação:
Inverter a placa e incubar em até15 minutos após a aplicação dos discos;
Incubação: 35±1ºC; 16-20h; Atmosfera normal;
Exceção 1 –Glicopeptídeos para Enterococcussp. – realizar leitura em 24h;
Exceção 2: Corynebacterium spp, Aerococcus e Kingella. Realizar leitura em 40-44h se crescimento insuficiente;
Exceção 3: Streptococcus spp, Haemophylus spp, Neisseria spp, outros fastidiosos em tensão de CO2 (4-6%).
– Leitura dos halos:
Superfície escura com luz posicionada diretamente sob a placa;
Auxílio de uma régua ou halômetro sobre o fundo da placa;
Meios com sangue – placa aberta – crescimento, não hemólise;
Leitura de oxacilina e vancomicina para Staphylococcus spp. e vancomicina para Enterococcus spp. deve ser feita sob uma luz transmitida.
– Apenas o CLSI define como Sensível dose dependente (SDD), para aquelas concentrações dependentes do regime de dose.
O BrCAST define a Área de Incerteza Técnica (AIT). Esta área corresponde a um valor de CIM e/ou intervalo de halo de inibição onde a categorização é incerta. Repetir o teste ou usar método alternativo (se houver dúvida quanto ao resultado). Modificar categoria se houver opções terapêuticas disponíveis ( com observação no laudo).
Temos ampla linha dos Discos de Antibiótico, bem como todos os meios de cultura indispensáveis para seus exames. Consulte-nos!

Referências:
Brazilian Committee on Antimicrobial Susceptibily Testing, BRCast. Orientações do EUCast/BRCast para a detecção de mecanismos de resistência e resistências específicas de importância clínica e/ou epidemiológica. Versão 2.0. Junho de 2017.











