por CenterLab | maio 22, 2022 | Informativos
A avaliação do estado ácido-básico do sangue é rotineiramente realizada na grande maioria dos doentes atendidos em Unidades de Terapia Intensiva (UTI), qualquer que seja a doença de base. Essa avaliação é fundamental, pois, além dos desvios do equilíbrio ácido-básico propriamente ditos, a gasometria pode fornecer dados sobre a função respiratória e sobre as condições de perfusão tecidual. Acidose e alcalose são modificações do pH sanguíneo decorrentes do aumento ou dadiminuição da concentração sanguínea de íons H+.
Normalmente no exame de gasometria são medidos o pH, a pressão de Oxigênio pO2 e a pressão de gás carbônico pCO2. Esses analitos são os principais componentes da gasometria, pois servem de base para calcular diversos outros parâmetros essenciais para reportar a condição do paciente. Alguns aparelhos são capazes de medir outros analitos junto aos parâmetros da gasometria, tais como: Glicose, Lactato, Hematócrito, Sódio, Potássio e Cálcio Iônico, que auxiliam o corpo clínico nas tomadas de decisões nas mais diversas situações de forma mais rápida e assertiva, a fim de assegurar os cuidados críticos com paciente.
Outros equipamentos dispõem ainda da detecção de dishemoglobinas (distúrbios em que a molécula de hemoglobina é funcionalmente alterada e impedida de transportar oxigênio). O método utilizado para medida da oxihemoglobina, desoxiemoglobina, carboxihemoglobina e metemoglobina é conhecido como CO-oximetria.
Sistema Tampão
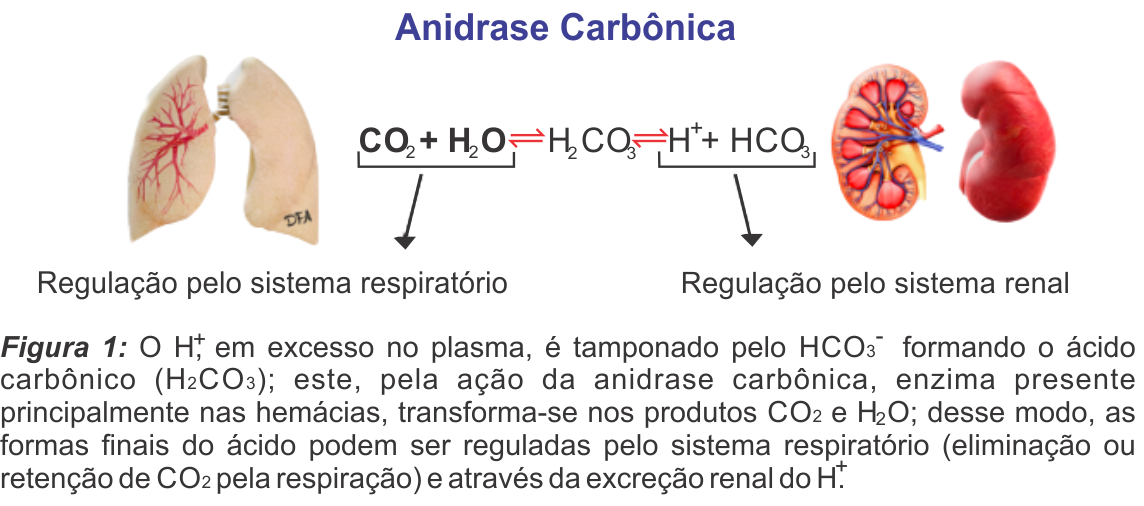
O sistema tampão é constituído pelo bicarbonato (HCO3- ), ossos, hemoglobina, proteínas plasmáticas e intracelulares. Estas substâncias são capazes de doar ou receber íons H minimizando alterações do pH e têm por objetivo deslocar a reação para maior produção de CO2 e água que podem ser eliminados pela respiração (Figura 1). O sistema tampão ocorre instantaneamente à alteração ácido-básica constituindo assim a primeira linha de defesa para variações do pH.
Componente Pulmonar
O controle pulmonar regula a concentração de CO2 sanguíneo através de sua eliminação ou retenção na acidose e alcalose, respectivamente. O controle respiratório é exercido por variações na concentração de íons H sobre o bulbo pulmonar. O componente pulmonar inicia-se minutos após a alteração ácido-básica, sendo o segundo componente na linha de defesa para variações do pH.
Componente Renal
Os rins controlam o equilíbrio ácido-básico ao excretarem urina ácida ou básica. Tal controle se dá através dos seguintes mecanismos: reabsorção de bicarbonato filtrado e regeneração do bicarbonato através da excreção de H ligada a tampões e na forma de amônio (NH4+ ).
Apesar de ser o terceiro componente na linha de defesa contra alterações do equilíbrio ácido-básico, levando horas a dias para agir, é o mais duradouro de todos os mecanismos regulatórios.
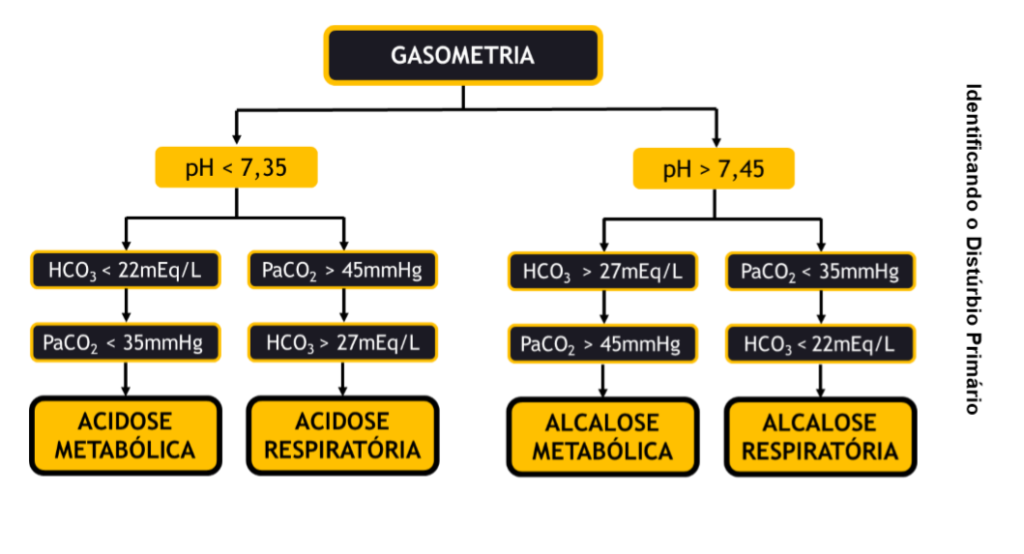
Distúrbios acido-básicos identificáveis na gasometria arterial
Temos inicialmente quatro distúrbios acidobásicos primários, dois metabólicos e dois respiratórios.
Acidose metabólica
Na acidose metabólica temos uma queda do HCO3 na gasometria e, consequentemente, redução do pH (acidose).
A resposta compensatória deve ser uma hiperventilação a fim de reduzir o CO2 (que também acidifica o meio).
Alcalose metabólica
Na alcalose metabólica, ocorre um aumento de HCO3 na gasometria e, consequentemente, elevação do pH (alcalose).
A resposta compensatória deve ser uma hipoventilação a fim de reter o Co2.
Acidose respiratória
Na acidose respiratória, existe uma dificuldade de ventilação do paciente, isso leva a uma hipoventilação e, consequentemente, retenção do Co2.
A resposta compensatória neste caso é renal (retém HCO3 ou excreção de mais ácido), com posterior elevação do HCO3 na gasometria.
Alcalose respiratória
Na alcalose respiratória, o paciente está hiperventilando e, consequentemente, “lavando” o CO2, isto é, expulsando o CO2. A resposta neste caso é renal com excreção de HCO3.
A Centerlab sempre empenhada em oferecer aos seus clientes as melhores soluções para o diagnóstico clínico, em parceria com a Werfen e Labtest, apresenta os equipamentos destinados à linha de “Acute Care Diagnostics” que trazem como características robustez, praticidade e qualidade nos resultados.
i15 – Labtest
Portátil, leve e de fácil operação, o sistema de gasometria i15 Labtest é a solução ideal para quem busca um sistema completo e versátil, que permite realizar análises em ambientes laboratoriais e hospitalares.
– Rapidez: Resultados em 48 segundos após a aspiração da amostra;
– Baixo volume de amostra: 140 uL;
– Seguro: Controle de qualidade em 3 níveis, Calibração automática a cada leitura de amostra;
– Portátil: Bateria de lítio, autonomia de 50 testes contínuos;
– Cartuchos Descartáveis: Test Cartridge BG10 – 25 testes
– Parâmetros Medidos:


Gem 3500 – Werfen
Adicionando à simplicidade, flexibilidade e confiabilidade de exames sem precedentes do GEM Premier 3000, o GEM Premier 3500 oferece novas capacidades em um sistema elevado, adaptável às necessidades – e volume – do seu hospital e laboratório.
– Simples: Livre de manutenção pelo usuário, multiuso, e menus intuitivos na tela sensível ao toque são muito fáceis de usar.
– Prático: Cartucho único, pack contendo todas as soluções necessárias para funcionamento, bem como a agulha de aspiração. Armazenamento em temperatura ambiente, garantindo melhor gerenciamento dos consumíveis.
– iQM: De propriedade da Werfen, a Gestão de Qualidade Inteligente (Intelligent Quality Management), providencia um controle de qualidade contínuo e em tempo real para os resultados mais precisos, o tempo todo. Equipamento executa automaticamente controles de qualidade, realizando, se necessário, ações corretivas (não contabiliza controle como teste). Tudo isso registrado em forma de relatórios e gráficos. O iQM é aprovado pelo FDA Americano e pelo Dr. Westgard, pioneiro na análise de controle de qualidade.
– Conectividade Total: O software GEMweb® permite a gestão de informações e comunicação em tempo real pelo hospital. Permite conexão via Wi-fi com a rede, espelhando a tela do aparelho, permitindo o acesso aos resultados remotamente bem como todos os gráficos de controle de qualidade.

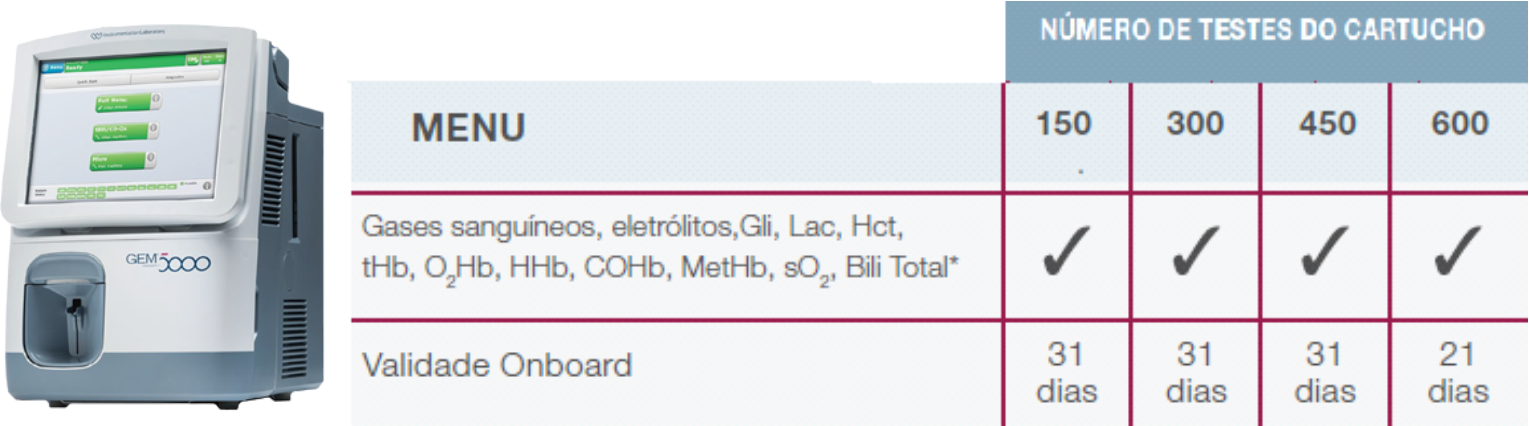
Gem 5000 – Werfen – Com Co-oximetria
O sistema de gasometria GEM Premier 5000 integra um sistema de garantia da qualidade automatizado para todas as amostras. Com sistema de gerenciamento Inteligente de Qualidade de segunda geração (iQM2) com tecnologia IntraSpect™, é possível identificar potenciais erros, não apenas antes e depois de cada análise, mas também durante o processamento de amostras.
O iQM2 realiza não só a identificação dos erros mas também inicia automaticamente a correção e a documentação em tempo real de todas as interferências detectadas.
Além disso, a usabilidade do analisador é bem simples e prática: basta substituir o GEM PAK (cartucho único que inclui todos os componentes necessários ao funcionamento do analisador), dependendo da sua rotina, até uma vez por mês.
Todas essas características juntas asseguram um resultado de qualidade e em conformidade para todas as amostras processadas no GEM Premier 5000.
Importante: Esse boletim tem o caráter informativo e não deve ser utilizado para interpretação de resultados e manejo clínico.
Referências:
– Interpretação de gasometria arterial. Eduardo Borges Gomes , Hugo Cataud Pacheco Pereira. Vittalle – Revista de Ciências da Saúde v. 33, n. 1 (2021) 203-218
– DISTÚRBIOS DO EQUILÍBRIO ÁCIDO-BÁSICO. Renato Marinho Furoni , Sinval Malheiros Pinto Neto , Rafael Buck Giorgi , Enio Marcio Maia Guerra . Rev. Fac. Ciênc. Méd. Sorocaba, v. 12, n. 1, p. 5 -12, 2010
– Gasometria Arterial: interpretação, parâmetros, distúrbios acidobásicos e mais! – Agosto 2018 – Disponível em < https://www.sanarmed.com/gasometria-arterial-como-interpretar> Acesso em 17/03/2022.
– Boletim Técnico & Científico Labtest – Gasometria e sua importância na avaliação dos pacientes críticos hospitalizados – Julho 2020 – Disponível em <https://labtest.com.br/gasometria-e-sua-importancia-naavaliacao- de-pacientes-criticos-hospitalizados/> Acesso em 17/03/2022.
– Folder I15 – Blood Gas Chemistry Analyzer – Labtest. | Folder Gem 3500 – Werfen | Folder Gem 5000 – Werfen

por CenterLab | maio 4, 2022 | Informativos
No corpo humano todas as células apresentam um ciclo natural, elas são originadas, diferenciam-se, proliferam e morrem. Entretanto, algumas células saem desse ciclo, evadindo-se dos mecanismos de controle celular, geralmente em decorrência de mutações. Consequentemente, essas células dão origem a outras células com as mesmas imperfeições transformando-se em um tumor. Os tumores apresentam duas características principais que os diferenciam, sendo, ritmo de crescimento (divisão celular) e sua capacidade de infiltração para outros tecidos. A palavra câncer é oriunda do latim, no qual o significado é caranguejo, devido sua capacidade invasiva. O termo já sugere seu caráter maligno, devido seu crescimento exacerbado e capacidade de migração. Este processo facilita a entrada dessas células em outros tecidos do corpo, podendo inclusive utilizar a corrente sanguínea ou sistema linfático como mecanismo de transporte, gerando assim, um tumor secundário ou metástase.
A leucemia, que vem do Grego LEUKOS, “branco”, mais HAIMA, “sangue”, são consideradas doenças malignas do sangue, ou seja, um tipo de câncer inicialmente originário na medula óssea, com consequências fisiológicas graves, podendo levar o indivíduo à morte. Nela ocorre a proliferação neoplásica generalizada ou acúmulo de células hematopoiéticas, com ou sem envolvimento do sangue periférico. Na maioria dos casos, as células leucêmicas (figura 1) extravasam para o sangue, onde podem ser vistas em grande número. Essas células também podem infiltrar o fígado, baço, linfonodos e outros tecidos. As leucemias podem ser agrupadas com base na velocidade em que a doença evolui e torna-se grave. Sob esse aspecto, a doença pode ser do tipo:
– Crônica (Caracterizada pelo aumento de células maduras, mas anormais). Nesse grupo, o câncer afeta majoritariamente as células que já passaram por certo processo de amadurecimento dentro da medula óssea e que já são mais desenvolvidas, de certa forma. No início da doença, as células leucêmicas ainda conseguem fazer algum trabalho dos glóbulos brancos normais. Geralmente descobrem se a doença durante exame de sangue de rotina. Lentamente, a leucemia crônica se agrava. À medida que o número de células leucêmicas aumenta, aparecem inchaço nos linfonodos (ínguas) ou infecções. Quando surgem, os sintomas são brandos, agravando-se gradualmente.
– Já a leucemia Aguda (caracterizam-se pela proliferação clonal acompanhada de bloqueio maturativo (anaplasia) variável. As células leucêmicas não podem fazer nenhum trabalho das células sanguíneas normais. O número de células leucêmicas cresce de maneira rápida e a doença agrava-se num curto intervalo de tempo.
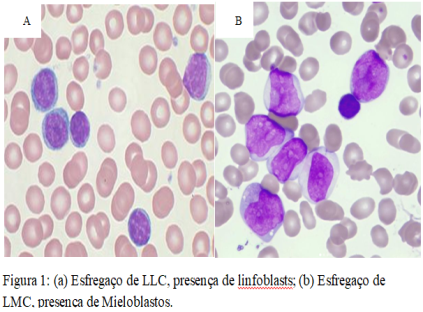
As leucemias também podem ser agrupadas baseando-se nos tipos de glóbulos brancos que elas afetam: linfoides ou mieloides. As que afetam as células linfoides são chamadas de linfoide, linfocítica ou linfoblástica. A leucemia que afeta as células mieloides são chamadas Mieloide ou mieloblástica. Combinando as duas classificações, existem quatro tipos mais comuns de leucemia:
– Leucemia Linfoide Aguda (LLA) – é o câncer mais comum na infância causado por uma mutação nos linfócitos na medula óssea por algum erro no DNA. Esse dano gera um linfoblasto que não amadurece e, por isso, não se transforma em uma célula sanguínea funcional.
– Leucemia Mieloide Aguda (LMA) – é o tipo mais comum e mais agressivo da doença. A LMA progride rapidamente, e as células mieloides interferem na produção normal de glóbulos brancos e vermelhos e de plaquetas. Tem predominância em adultos mais velhos (acima de 60 anos de idade), com mais de 50% dos casos. É mais comum no sexo masculino do que no feminino, representa cerca de 15% a 20% das LA da infância e 80% das dos adultos e apresenta um prognóstico ruim, especialmente em pacientes idosos.
– Leucemia Linfoide crônica (LLC) – é caracterizada pelo acúmulo progressivo de linfócitos B malignos fenotipicamente maduros.Os locais primários da doença incluem sangue periférico, medula óssea, baço e linfonodos. Ela progride lentamente e costuma afetar idosos e é o tipo mais comum de leucemia no mundo ocidental.
– Leucemia Mieloide Crônica (LMC) – nesse tipo de leucemia, o corpo produz um grande número de células anormais da série Mieloide. Essas contagens vão aumentando de forma progressiva. É causada por uma mutação de cromossomos que ocorre espontaneamente. É comum ocorrer o aumento do baço associado, chamado de esplenomegalia.
Para o ano 2030, a Organização Mundial da Saúde (OMS) estimou 75 milhões de pessoas vivas com câncer, sendo 21 milhões de casos novos da doença e 13 milhões de mortes em todo mundo. Atualmente, a estimativa é de 14 milhões de casos novos e 8 milhões de mortes por câncer. O Instituto Nacional de Câncer (INCA) estima que, para cada ano do triênio 2020/2022, sejam diagnosticados no Brasil 5.920 casos novos de leucemia em homens e 4.890 em mulheres.
As causas da leucemia ainda não estão definidas, mas, suspeita-se da associação entre determinados fatores com o risco aumentado de desenvolver alguns tipos específicos da doença como: tabagismo, Síndrome de Down e outras doenças hereditárias, Síndrome mielodisplásica e outras doença sanguíneas, benzeno, radiação ionizante (raios X e gama), quimioterapia (algumas classes de medicamentos usados no tratamento do câncer e doenças auto-imunes), formaldeído, produção de borracha, história familiar, idade, exposição a agrotóxicos, solventes, diesel, poeiras, infecção por vírus de hepatite B e C.
Sintomas:
Os primeiros sinais geralmente aparecem quando a medula óssea deixa de produzir células sanguíneas normais. Tendo com principais sintomas palidez, cansaços, palpitações, gânglios aumentados, infecções persistentes ou recorrentes, hematomas, manchas avermelhadas pelo corpo, sangramentos incomuns, aumento do baço e do fígado, anemia, fraqueza, febre ou suores noturnos; perda de peso sem motivo aparente, dores nos ossos e nas articulações, dores de cabeça, náuseas, vômitos, visão dupla e desorientação.
Tratamento:
O tratamento vai desde quimioterápico ou medicamentos direcionados que eliminam especificamente as células cancerígenas até transplante de medula óssea.
Diagnóstico:
Diante da suspeita de um quadro de leucemia, um dos principais exames de sangue para confirmação é o hemograma. Em caso positivo, o hemograma estará alterado, mostrando na maioria das vezes um aumento do número de leucócitos (na minoria das vezes o número estará diminuído), associado ou não à diminuição das hemácias e plaquetas. Outras análises laboratoriais devem ser realizadas, como exames de bioquímica e da coagulação, e poderão estar alterados.
A confirmação diagnóstica é feita com o exame da medula óssea (mielograma). Entretanto o hemograma de uma pessoa com leucemia que apresenta alteração pode auxiliar no diagnóstico. É possível que elas apareçam em um curto intervalo de tempo e ajudem a identificar, precocemente, esse tipo de câncer. No caso das leucemias agudas, ou seja, a leucemia mieloide aguda (LMA) e leucemia linfoide aguda(LLA) há três principais elementos que devem ser analisados. A hemoglobina, as plaquetas e se há presença dos blastos. Caso o resultado do hemograma indique que o nível de hemoglobina está baixo (menor que 12g/dl), plaquetas baixas (menor que 100.000/mm³) e mais de 20% de blastos, há uma grande probabilidade de ser uma leucemia aguda. Já o hemograma de uma pessoa com leucemia crônica será diferente, dependendo do tipo de leucemia. Isso acontece porque cada subtipo apresenta um conjunto de alterações no exame de sangue. Na LMC, o nível de leucócitos é alto com aparecimento de leucócitos jovens. Sendo que há uma maior quantidade de elementos jovens em comparação com os mais velhos, chamado de desvio escalonado. Enquanto que na LLC, há um aumento de 40% dos linfócitos em comparação com o hemograma de uma pessoa saudável. Nesta situação o aumento dos linfócitos indica a presença de anomalia nestas células. A confirmação é feita pela imunofenotipagem e marcadores moleculares.
O progresso das tecnologias médicas recentes é notável. Em hematologia, muitos resultados da medição são processados automaticamente em sistemas de alto rendimento. A Centerlab, comprometida em oferecer o melhor em automação laboratorial, juntamente com a Nihon Kohden, empresa Japonesa com 40 anos de experiência na fabricação de analisadores hematológicos, apresenta sua linha equipamentos. Máquinas robustas fabricadas em aço inoxidável, de fácil operação pelo usuário, toda linha de equipamentos possui um sistema de filtros e limpeza automática para retenção e remoção de coágulos. Tudo isso além de tecnologias exclusivas da Nihon Khoden que trazem maior rapidez, segurança e qualidade no diagnóstico de doenças hematológicas.
Tecnologias Exclusivas Nihon Kohden:
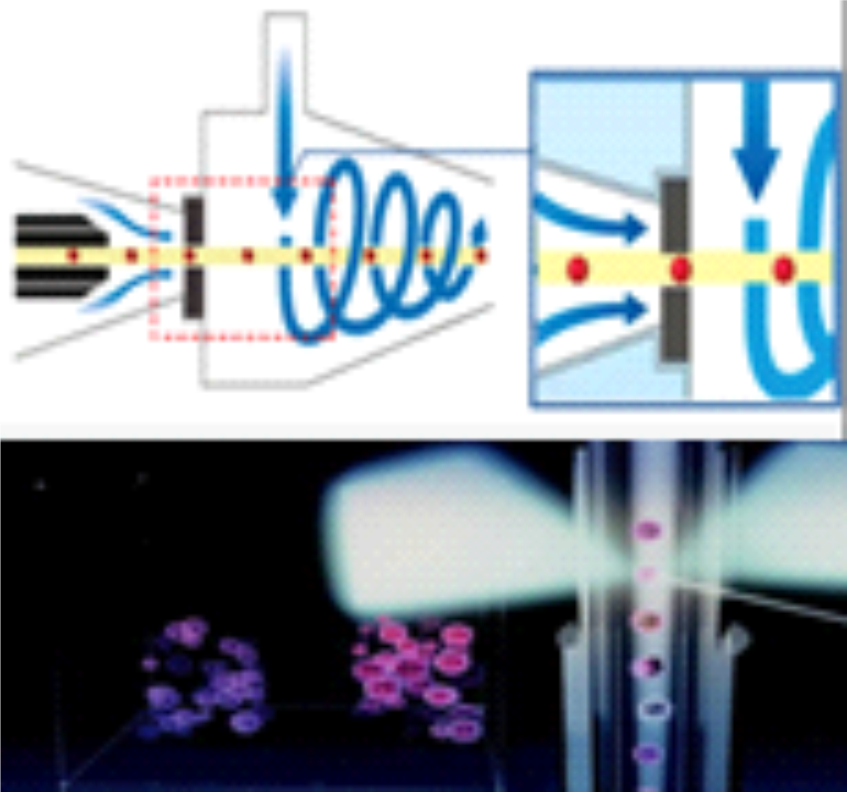
A tecnologia ótica ”DynaScatter Laser” (presentes no Celltac ES e Celltac G) analisa e diferencia as células WBC em seu estado “quase-nativo” com muita precisão. O inovador sistema de detecção de espalhamento de laser de 3 ângulos provê uma melhor diferenciação dos Leucócitos realizando uma medição precisa. A tecnologia chamada “DynaHelix Flow” (presente no Celltac G) alinha perfeitamente as células Leucócitos, Hemácias e Plaquetas para uma contagem de alta impedância com precisão usando um fluxo hidrodinâmico focado antes de passar pela abertura. Somado a isso, o fluxo contínuo após a contagem previne totalmente contra o risco de a mesma célula ser contada duas vezes (retorno).
Celltac α 6550
– Tecnologia Japonesa, velocidade de60 amostras/hora e volume de amostra: 30 microL;
– 19 Parâmetros: WBC, RBC, HGB, HCT, MCV, MCH, MCHC, RDW-CV, RDW-SD, PLT, PCT, MPV, PDW;
– Diferencial de Leucócitos em 3 partes (LY, LY%, MO, MO%, e GR, GR%)*;
– Verificação diária automática e livre de manutenção, gerenciamento da utilização dos reagentes, análise em tubo aberto e fechado,eliminando contato com sangue (biosegurança) e impressora térmica integrada;
– Remoção automática de coágulos, filtros de retenção de coágulos, compacto, durável, robusto todo em aço inox.
Celltac ES
– Tecnologia Japonesa, velocidade de60 amostras/hora e volume de amostra: 55μl;
– 25 Parâmetros: WBC, RBC, HGB, HCT, MCV, MCH, MCHC, RDW-CV, RDW-SD, PLT, PCT, MPV, PDW;
– Diferencial de Leucócitos 6 partes: LY, LY%, MO, MO%, NE, NE%, EO, EO%,BA, BA%, IG, IG%;
– Verificação diária automática e livre de manutenção, gerenciamento da utilização dos reagentes e análise em tubo aberto e fechado, eliminando contato com sangue (biosegurança);
– Contagem avançada de PLT e WBC para valores baixo automaticamente e impressora térmica integrada;
– Remoção automática de coágulos, filtros de retenção de coágulos e compacto, durável, robusto todo em aço inox.
Celltac G 9100
– Tecnologia Japonesa, velocidade de 90 amostras/hora e volume de amostra: 40 microL;
– 33 Parâmetros: WBC, RBC, HGB, HCT, MCV, MCH, MCHC, RDW-CV, RDW-SD, PLT, PCT, MPV, PDW, P-LCR, PLCC, Índice Mentzer e RDW-I;
– Diferencial de Leucócitos 7 partes: LY, LY%, MO, MO%, NE, NE%, EO, EO%,BA, BA%, Band, Band%, IG, IG%, Seg% e Seg;
– Verificação automática e livre de manutenções diárias, extremamente fácil operação, valores de controles adicionados automaticamente por cód. de barras, Carregamento continuo de amostras com capacidade para 7 racks de 10 tubos e jomogeneização e análise automática das amostras (tubo fechado);
– Gerenciamento e rastreabilidade dos reagentes;
– Remoção automática de coágulos, filtros de retenção de coágulos, compacto, durável, robusto todo em aço inox;
– Os recém adicionados RDWI e Índice Mentzer adicionam valiosas informações clínicas para que se possa diferenciar beta-talassemia de uma possível anemia ferropriva nos casos de anemia microcítica.

Importante: Esse boletim tem o caráter informativo e não deve ser utilizado para interpretação de resultados e manejo clínico.
Referencias:
– http://www.oncoguia.org.br/conteudo/sinais-e-sintomas-da-leucemia-mieloide-aguda-lma/1598/332/
– https://www.rededorsaoluiz.com.br/clinica/cehon/sobre-o-cancer/neoplasias-hemat/leucemia-cronica
– https://www.msdmanuals.com/pt-br/profissional/hematologia-e-oncologia/leucemia/leucemia-linfoc%C3%ADtica-cr%C3%B4nica-llc
– https://www.scielosp.org/article/csc/2017.v22n10/3321-3332/
– https://portal.unisepe.com.br/unifia/wp-content/uploads/sites/10001/2019/02/022_LEUCEMIA-MIELOIDE-AGUDA-E-CR%C3%94NICA-DIAGN%C3%93STICOS-E-POSS%C3%8DVEIS-TRATAMENTOS.pdf
– https://www.scielo.br/j/jbpml/a/C6NQ7KQYbZNsdpp7TGW7vpk/?format=pdf&lang=pt
– https://www.inca.gov.br/tipos-de-cancer/leucemia
– https://revista.abrale.org.br/hemograma-e-diagnostico-de-leucemia/
– https://bvsms.saude.gov.br/bvs/publicacoes/inca/Avaliacao_epidemiologica_das_leucemias_linfoblasticas_em._pa.pdf
– https://www.einstein.br/especialidades/oncologia/tipos-cancer/leucemia

por CenterLab | abr 18, 2022 | Informativos
A anemia é definia pela Organização Mundial de Saúde (OMS) como a condição na qual o conteúdo de hemoglobina no sangue está abaixo do normal, resultando em uma redução na capacidade de transportar o oxigênio.
Os sintomas mais importantes da anemia são: fadiga, letargia, mal-estar ou tontura, pode ocorrer também dores de cabeça, falta de ar, irritabilidade, queda de cabelo, síndrome das pernas inquietas e unhas quebradiças.
As anemias podem ser agudas ou crônicas e essas adquiridas ou hereditárias:
As agudas ocorrem quando há perda acelerada e expressiva de sangue, o que pode acontecer nos acidentes, cirurgias, etc.
Já as anemias crônicas são provocadas por alguma doença de base, podendo ser:
– Adquirida como as que ocorrem por deficiência nutricional, na gestação, por carência de Vitamina B12 ou Ácido Fólico (anemia megaloblástica) ou a mais comum por deficiência de ferro (anemia ferropriva).
– Hereditárias por alguma alteração genética que modifica e compromete o funcionamento normal das hemoglobinas ou a formação normal das hemácias, como nas Talassemias e anemia falciforme, respectivamente.
Dados recentes do Estudo Nacional de Alimentação e Nutrição Infantil (ENANI 2019) apontam que no Brasil prevalências de anemia e anemia ferropriva foram de 10,0% e 3,5%, respectivamente.
Classificação Laboratorial das Anemias
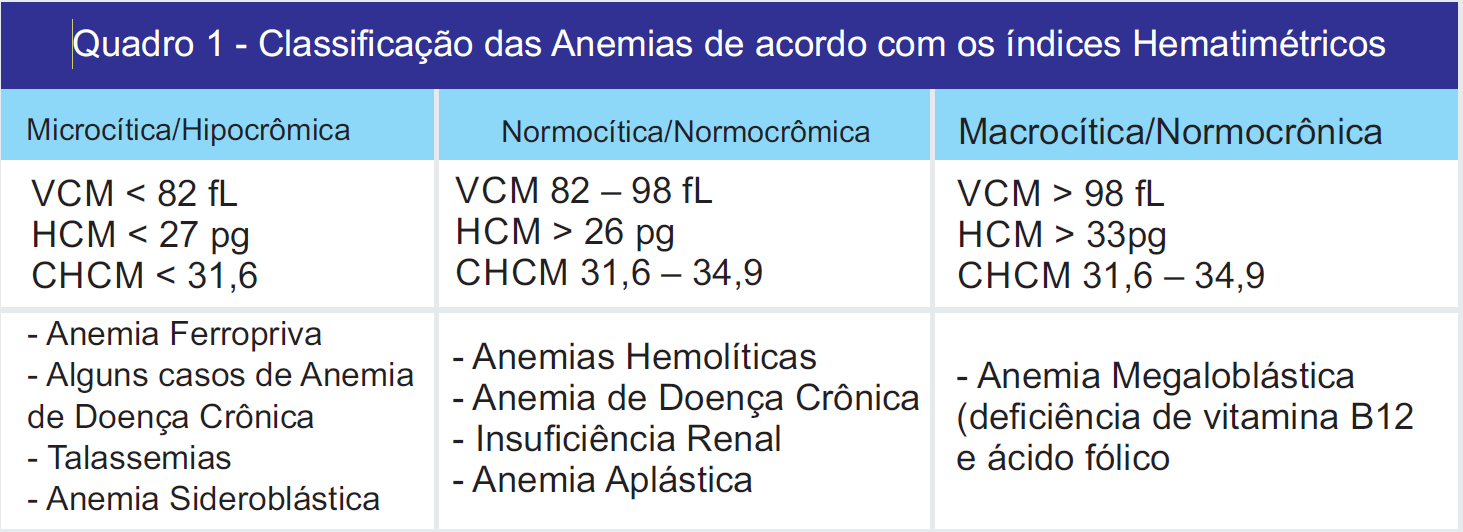
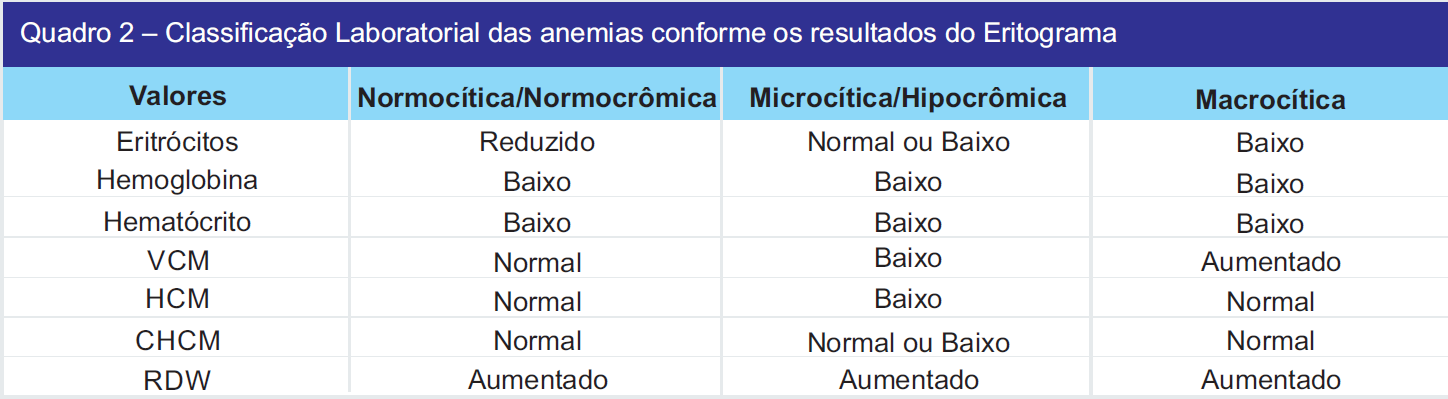
Os índices hematimétricos são parâmetros fornecidos pelo hemograma quando esse exame é realizado em equipamentos automatizados e auxiliam no diagnóstico das diferentes anemias (Quadro 1). A classificação laboratorial das anemias de acordo os resultados do eritograma está representada no Quadro 2.
Volume Corpuscular Médio (VCM), Hemoglobina Corpuscular Média (HCM), Concentração de Hemoglobina Corpuscular Média (CHCM) e Coeficiente de Distribuição das Hemácias (RDW), permitem classificar as anemias decorrentes de diferentes causas em três classes:
– Anemia Normocítica/Normocrômica:
São causadas pela menor produção ou destruição de eritrócitos.
– Anemias por doença crônica: Caracterizada pelo desenvolvimento de anemia em pacientes com doenças crônicas.
– Anemias hemolíticas: Se caracterizam por lise ou destruição dos eritrócitos pelas células do sistema retículo endotelial
presentes no baço, fígado e medula óssea. Podem ser autoimunes ou genéticas.
– Anemia aplástica: Se desenvolve como resultado de danos à medula óssea.
– Anemia Microcítica/Hipocrômica:
Dentre as anemias microcíticas e hipocrômicas destacam-se:
– Anemia Ferropriva: É a mais comum, ocorre geralmente devido a inadequada ingestão, absorção ou pelo aumento da necessidade de Ferro durante o período gestacional ou durante o período de crescimento. Também pode se desenvolver em decorrência do período menstrual, presença de parasitas intestinais e hemorragias.
– Talassemias: A talassemia é uma hemoglobinopatia de caráter genético e hereditário, é uma condição clínica caracterizada pela ausência ou redução da síntese de cadeias globínicas tipo alfa (α) ou tipo beta (β), subunidades que compõe a molécula da hemoglobina.
– Anemia Macrocítica/Normocrômica:
Dentre as anemias macrocíticas a mais frequente é a anemia megaloblástica, uma anemia decorrente da deficiência de vitamina B12 e/ou de ácido fólico e é caracterizada por defeitos na síntese de DNA.
A Centerlab, comprometida em oferecer o melhor em automação laboratorial, juntamente com a Nihon Kohden, empresa com 40 anos de experiência na fabricação de analisadores hematológicos, apresenta sua linha equipamentos. Máquinas robustas fabricadas em aço inoxidável, de fácil operação pelo usuário, toda linha de equipamentos possui um sistema de filtros e limpeza automática para retenção e remoção de coágulos. Tudo isso além de tecnologias exclusivas da Nihon Khoden trazem maior rapidez, segurança e qualidade no diagnóstico de doenças hematológicas.
Tecnologias Exclusivas Nihon Kohden
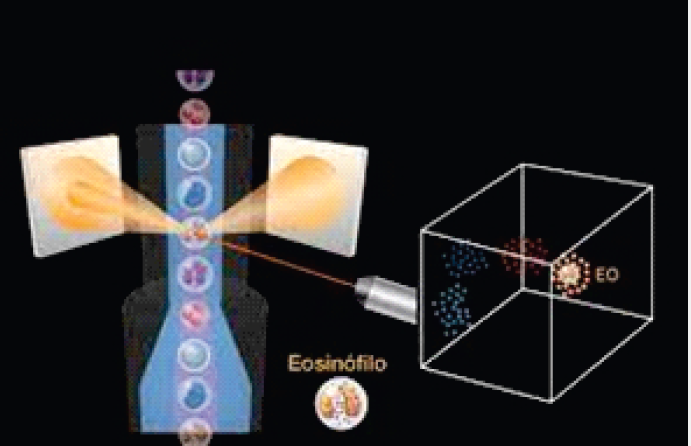
A tecnologia ótica ”DynaScatter Laser” (presentes no Celltac ES e Celltac G) analisa e diferencia as células WBC em seu estado “quase-nativo” com muita precisão. O inovador sistema de detecção de espalhamento de laser de 3 ângulos provê uma melhor detecção de WBC realizando uma medição precisa.
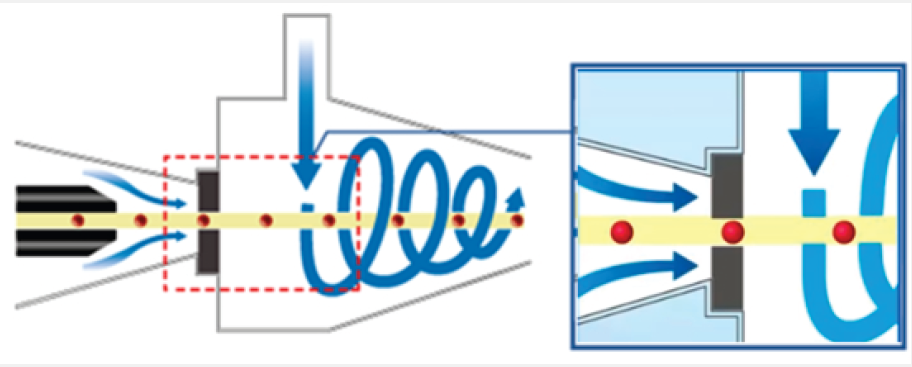
A tecnologia chamada “DynaHelix Flow” (presente no Celltac G) alinha perfeitamente as células WBC, RBC e PLT para uma contagem de alta impedância com precisão usando um fluxo hidrodinâmico focado antes de passar pela abertura. Somado a isso, o fluxo contínuo após a contagem previne totalmente contra o risco de a mesma célula ser contada duas vezes (retorno).
Celltac α
Principais caracteristicas:
– Tecnologia Japonesa;
– Velocidade: 60 amostras/hora;
– Volume de amostra: 30 microL;
– 19 Parâmetros: WBC, RBC, HGB, HCT, MCV, MCH, MCHC, RDW-CV, RDW-SD, PLT, PCT, MPV, PDW;
– Diferencial de Leucócitos em 3 partes (LY, LY%, MO, MO%, e GR, GR%)*;
– Verificação diárias automáticas e livres de manutenção;
– Gerenciamento da utilização dos reagentes;
– Análise em tubo aberto e fechado, eliminando contato com sangue (biosegurança);
– Impressora térmica integrada;
– Utiliza 3 reagentes: Isotonac, Hemolynac-3N e Cleanac (Cleanac 3 apenas para limpeza pesada, 1 vez por semana).
– Remoção automática de coágulos;
– Filtros de retenção de coágulos;
– Compacto, durável, robusto todo em aço inox.
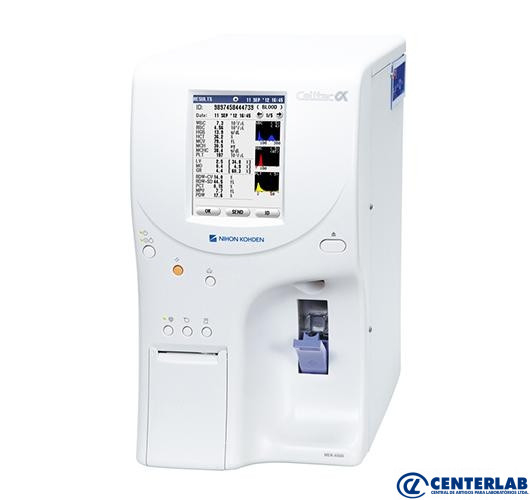
Celltac ES
Principais caracteristicas:
– Tecnologia Japonesa;
– Velocidade: 60 amostras/hora;
– Volume de amostra: 55 microL;
– 25 Parâmetros: WBC, RBC, HGB, HCT, MCV, MCH, MCHC, RDW-CV, RDW-SD, PLT, PCT, MPV, PDW;
– Diferencial de Leucócitos 6 partes: LY, LY%, MO, MO%, NE, NE%, EO, EO%,BA, BA%, IG, IG%
– Verificação diárias automáticas e livres de manutenção.
– Gerenciamento da utilização dos reagentes.
– Análise em tubo aberto e fechado, eliminando contato com sangue (biosegurança);
– Contagem avançada de PLT e WBC para valores baixo automaticamente;
– Impressora térmica integrada
– Utiliza 4 reagentes: Isotonac, Hemolynac-3N, Hemolynac-5 e Cleanac (Cleanac 3 apenas para limpeza pesada, 1 vez por semana).
– Remoção automática de coágulos.
– Filtros de retenção de coágulos.
-Compacto, durável, robusto todo em aço inox.

Celltac G
Principais caracteristicas:
– Tecnologia Japonesa;
– Velocidade: 90 amostras/hora;
– Volume de amostra: 40 microL;
– 33 Parâmetros: WBC, RBC, HGB, HCT, MCV, MCH, MCHC, RDW-CV, RDW-SD, PLT, PCT, MPV, PDW, P-LCR, PLCC,
Índice Mentzer e RDW-I;
– Diferencial de Leucócitos 7 partes: LY, LY%, MO, MO%, NE, NE%, EO, EO%,BA, BA%, Band, Band%, IG, IG%,
Seg% e Seg.
– Verificação automática e livre de manutenções diárias, extremamente fácil operação.
– Valores de controles adicionados automaticamente por cód. de barras.
– Carregamento continuo de amostras com capacidade para 7 racks de 10 tubos.
– Homogeneização e análise automática das amostras (tubo fechado);
– Gerenciamento e rastreabilidade dos reagentes;
– Utiliza 4 reagentes: Isotonac, Hemolynac-310, Hemolynac-510, Cleanac 710 (Cleanac 810 apenas para limpeza pesada, 1 vez por
semana).
– Remoção automática de coágulos.
– Filtros de retenção de coágulos.
– Compacto, durável, robusto todo em aço inox.

Referências:
– Silva, Andréa Gomides. Prevalência de anemias nos pacientes atendidos pelo LAPAC no período de 2016 a 2017 [manuscrito]. Universidade Federal de Ouro Preto. Escola de Farmácia. Departamento de Farmácia – 2018.
– Abreu, Ronaldo Palhares. Metabolismo da hemoglobina e Classificação das Anemias. Disponível em < https://slideplayer.com.br/slide/9541431/> acesso em 29/03/2022.
– Brasil. Ministério da Saúde. Secretaria de Atenção à Saúde. Departamento de Atenção Básica. Programa Nacional de Suplementação de Ferro : manual de condutas gerais / Ministério da Saúde. Secretaria de Atenção à Saúde. Departamento de Atenção Básica. Brasília: Ministério da Saúde, 2013.
– Relatório 3 – “Biomarcadores do Estado de Micronutrientes” – Estudo Nacional de Alimentação e Nutrição

por CenterLab | abr 9, 2022 | Informativos
Como limpar o celular para se proteger do Coronavírus?
Com a pandemia de Coronavírus que vem atingindo o mundo, alguns cuidados têm sido intensificados para evitar a contaminação pelo vírus: uso de álcool em gel, máscaras para evitar o contágio e a restrição de contato com outras pessoas como cumprimentos, por exemplo, foram algumas medidas adotadas para conter os efeitos do COVID-19.
O Coronavírus que pode ser transmitido pelo contato, desde que o vírus esteja naquela superfície. E com tanta preocupação com o contato entre as pessoas, acabamos esquecendo que ele pode estar em outros lugares como maçanetas, barras nos transportes públicos, teclados, celulares e outros locais.
Uma dica para quando você tiver que ir ao mercado, padaria ou farmácia, ao invés de pagar com o cartão de crédito em plástico, em que você precisa inserir na maquininha e digitar a senha, que tal pagar através de um aplicativo, tal como Google Pay ou Apple Pay? Dessa forma basta você aproximar o celular da maquininha, sem a necessidade de contato físico.
Mas depois que chegamos em casa, é que surge a dúvida: Como limpar o celular para se proteger do Coronavírus? Confira as dicas a seguir!
Como limpar o celular para se proteger do Coronavírus?
Para fazer a limpeza de um celular da maneira correta, é importantes ter alguns cuidados. Tenha uma flanela limpa e macia, evitando causar danos na tela ou arranhar outro componente de seu smartphone. Para fazer a higienização adequada aparelhos eletrônicos, o recomendado é utilizar o álcool isopropílico 70%.
Fabricantes como Apple e Samsung recomendam o uso deste componente para desinfectar telas e teclados, pois o álcool isopropílico evita danos por oxidação que outros produtos com água em sua composição possam causar.
Entretanto, você pode usar o álcool em gel ou o álcool etílico para limpar componentes externos, como a capinha do celular por exemplo. Para esse tipo de acessório, os especialistas recomendam a higienização por três vezes ao dia.
Outras dicas importantes para se proteger do Coronavírus
– Utilize comandos de voz
Na tentativa de diminuir os contatos entre as pessoas, cumprimentos foram reinventados. Ao invés do tradicional aperto de mãos, saudações usando os cotovelos, como mostra na alteração de logo do Mercado Livre, ou até mesmo utilizando os pés são maneiras encontradas.
E para diminuir o toque nas telas de celulares, recorrer a comandos de voz é uma alternativa. Cada vez mais, os assistentes de voz têm evoluído e com respostas mais inteligentes e rápidas, então você pode utilizar dessa funcionalidade para diminuir o contato em superfícies e a chance de contaminação pelo Coronavírus.
– Aplicativos para evitar aglomerações
Uma das facilidades que a tecnologia trouxe foi o crescimento no uso de aplicativos.
E com o cenário de pandemia de Coronavírus, utilizar aplicativos para atividades simples do cotidiano para evitar concentrações é uma forma de blindar-se, principalmente se você estiver em um dos grupos mais vulneráveis.
Produtos ligados à alimentação, medicamentos e outros itens básicos lideram os pedidos nos principais aplicativos.
– Atualização direto de sua casa
Uma outra maneira de usar a tecnologia ao ser favor nesse cenário com o Coronavírus é aproveitar o tempo para estudar a distância, mantendo seu desenvolvimento em constante evolução.
Fonte: comschool
por CenterLab | mar 14, 2022 | Informativos
Uso de novas preparações de heparina para eliminar a interferência nas Medições de cálcio ionizado: todos os problemas foram resolvidos?
Uma antiga preocupação na medição rápida de cálcio ionizado é a interferência da heparina usada como anticoagulante. Embora o soro possa ser obtido e analisado sem o uso de anticoagulante, a coagulação e a centrifugação aumentam o tempo de resposta e podem apresentar resultados variáveis (1, 2). É necessário pouco heparina (~ 1 UI/mL) para inibir a coagulação. Uma molécula de heparina catalisa a ligação entre muitas moléculas de antitrombina III e trombina, impedindo assim a conversão de fibrinogênio em fibrina.
A “heparina líquida” (isto é, heparina em solução) mistura-se prontamente com o sangue, contudo, o uso de heparina líquida em dispositivos de coleta de sangue está em declínio por vários motivos. Atualmente os equipamentos são desenvolvidos para analisar gases no sangue, eletrólitos, glicose, lactato, magnésio, etc, no sangue total, e a adição de heparina líquida pode causar erros de diluição nesses outros testes. Portanto, o anticoagulante ideal seria o seco, livre de interferências em testes de laboratório, baixo custo e completamente confiável como anticoagulante. Embora a heparina liofilizada não produza uma diluição do sangue, é necessário tempo de exposição ao anticoagulante para que ele se dissolva e se misture completamente com o sangue para inibir a coagulação. Pequenas bolhas de ar retidas, podem impedir o contato da heparina com o sangue e, portanto, a sua dissolução. Consequentemente, quantidades maiores de heparina liofilizada (do que “liquida”) são geralmente usadas em seringas para garantir que heparina suficiente seja dissolvida.
Os sais de heparina tal como sódio ou lítio têm sido usados na forma líquida e liofilizada como substâncias anticoagulantes por muitos anos; no entanto, a ligação de íons de cálcio à heparina pode reduzir artificialmente a concentração de cálcio ionizado em uma quantidade proporcional à concentração de heparina. Por exemplo, 15 UI de heparina de sódio por mililitro de sangue diminui a medição de cálcio ionizado em ~ 0,03 mmol/L; já, 25 UI/ml, reduz o cálcio ionizado em ~ 0,05 mmol/L.
Para minimizar ou eliminar a interferência da heparina nos resultados de cálcio ionizado, muitas preparações de heparina modificadas foram desenvolvidas. Heparinas líquidas tituladas com cálcio foram produzidas pela Radiometer no final da década de 70. Este produto praticamente eliminou qualquer efeito nos resultados de cálcio ionizado em concentrações de 1,0-1,5 mmol/L, mas, fora desse intervalo, aumentou ligeiramente os resultados mais baixos de cálcio ionizado e diminuiu ligeiramente resultados mais altos de cálcio ionizado, ambos em ~ 0,03 mmol/L. Estas alterações são devidas à quantidade relativamente grande de heparina de cálcio presente, que foi projetada para ter um valor normal de cálcio ionizado. Embora essas alterações tenham pouca consequência clínica na maioria das situações, a heparina titulada com cálcio líquido deve ser adicionada manualmente ao dispositivo de coleta de sangue, tornando o produto impraticável para uso rotineiro.
Mais recentemente, a heparina balanceada com cálcio (eletrólito) tornou-se disponível em seringas. Em uma avaliação desse produto (1), Smooth E (Radiometer), mostrou que os resultados de cálcio ionizado estavam dentro de ± 0,02 mmol/L de resultados de sangue total não coagulado com concentrações de cálcio ionizado variando de 0,90 a 1,60 mmol/L. No entanto, como no produto líquido, os valores de cálcio ionizado abaixo desse intervalo aumentaram levemente e os valores acima desse intervalo diminuíram levemente pela presença da heparina. Além disso, os resultados totais de cálcio foram aumentados em uma média de 0,06 mmol/L (1).
Na mesma época, Marquest produziu uma seringa (Gas-Lyte) que continha apenas 2-3 UI de heparina por mililitro. O novo aspecto deste produto foi o fato da heparina ser preparada em um material inerte com duas propriedades importantes: (a) a solução de heparina dissolveu-se rapidamente e presumivelmente foi dispersada por toda a amostra com uma mistura adequada; (b) a solução de heparina pode ser dispersada durante a produção para fornecer uma quantidade precisa de heparina para cada seringa. Os cristais “puros” da heparina de lítio não podem ser dispersados com tanta precisão. Outro produto foi desenvolvido recentemente, com heparina para uso com medições de cálcio ionizado, é a heparina de zinco. A justificativa para o desenvolvimento deste produto é que (a) os íons de zinco, ao se ligarem a locais de ligação de cátions bivalentes na heparina, impedem a ligação por íons de cálcio, (b) as concentrações de cálcio ionizadas baixas e altas não são afetadas, e (c) os resultados totais de cálcio não são afetados. Embora essas condições parecem ser atendidas, a presença de excesso de íons de zinco causa interferência positiva em ambas determinações de cálcio ionizado (3) e nas medições de magnésio total por métodos amplamente utilizados (4).
Como a heparina de lítio reduz o cálcio ionizado e a heparina de zinco aumenta o cálcio ionizado, foi desenvolvida a heparina de zinco e lítio neutralizada com cálcio (CNLZ) (Sherwood Medical Co.). Como mostra Landt et al. (3) nesta edição, este produto praticamente elimina efeitos sobre cálcio ionizado, cálcio total, potássio, sódio, pH, PCo2 e Po2. No meu laboratório, também avaliamos um produto similar da Martell Medical Co. que não influencia o cálcio ionizado (não publicado).
Embora esses produtos de heparina de lítio-zinco ofereçam uma quantidade relativamente alta de heparina sem os problemas encontrados anteriormente, Wilhite et al. (4) relatam (veja a edição do próximo mês) que a heparina pura de zinco interfere no magnésio total plasmático medido por equipamento amplamente usado. Se o sangue coletado em seringas em que ambas contenham lítio e heparina de zinco estará sujeito a interferências significativas com o magnésio. Tais medidas ainda precisam ser determinadas.
Swanson et al. (5) compararam seis métodos de coleta de cálcio ionizado. (e para Na, K e pH). A seringa de Gas- Lyte contendo 2,8 UI/mL de heparina dispersa em uma camada inerte de carga não mostrou viés no cálcio ionizado comparados com amostras coletadas sem heparina.
A concentração muito baixa de heparina dessas seringas deve causar pouca ou nenhuma interferência na maioria dos testes de laboratório, dado o lítio. A heparina a 15 UI/mL é usada há anos em amostras testadas para analitos químicos de rotina. Uma preocupação com este produto é que, em uso rotineiro, a baixa quantidade de heparina pode ser insuficiente para evitar a coagulação em todas as amostras. No entanto, tanto a nossa avaliação (não publicada), como a de Swanson et al. (5), bem como o uso rotineiro em um grande centro médico por mais de dois anos (comunicação pessoal, Donald Forman, Hospital Memorial da Carolina do Norte, Chapei Hill, NC) não indicaram que a coagulação de amostras seja um problema. No entanto, deve-se ter em mente que este produto contém uma propriedade inerte de enchimento que pode potencialmente interferir em outros testes laboratoriais de rotina.
Estão disponíveis pelo menos três tipos de produtos para seringas que contêm novas preparações de heparina que praticamente eliminam a interferência da heparina na medição de cálcio ionizado. Outros anticoagulantes como por exemplo, hirudina recombinante (6), parecem não ter efeito no cálcio ionizado medido. Dado que algumas das preparações de heparina parecem afetar outros testes – por exemplo, cálcio total. (1) e magnésio. (4) – será importante testar esses novos anticoagulantes quanto a seus efeitos em testes químicos de rotina que possam ser solicitados em amostras coletadas principalmente para cálcio ionizado e (ou) medição de gases no sangue. Como atualmente essa combinação de solicitação é relativamente incomum, uma interferência em algumas análises não impede necessariamente o uso do anticoagulante. No entanto, esforços contínuos para minimizar a quantidade de sangue coletado, principalmente em pacientes pediátricos e idosos, podem aumentar a frequência do requerimento para testes adicionais em amostras originalmente coletadas para análises de cálcio ionizado / gases sanguíneos.
Referências:
1. Toff’aletti J, Ernst P, Hunt P, Abrams B. Dry electrolytebalauced heparinized syringes evaluated for determining ionized calei.um and other electrolytes in whole blood. Clin Chem 1991;37: 1730–3.
2. Urban P, Buchmann B, Scheidegger D. Facilitated determinatiou of ionized calei.um. Clin Chem 1985;31:264–6.
3. Landt M, Hortin GL, Smith CH, McClellan A. Scott MG. luterfereDCe in ionized calei.um measurements by heparin salta. Clin Chem 1994;40:566-70.
4. Wilhit.e TR, Smith CH, Landt M. Interference of zinc heparin anticoagulant in plasma magnesium determinatiou. Clin Chem 1994;40: in presa.
5. Swanson JR, Heet.er C, IJrnboeker M, Sullivan M. Bias of ionized calcium result.s for blood gas syringes [Letter]. Clin Chem 1994;40:677-78.
6. Fareecl J, Walenga JM, lyer L, Hoppensteadt D, Pifarre R. An objective perspective on recombinant hirudin: A new anticoagulant and antithrombotic agent. Blood Coag Fibrinolysis 1991;2: 113-20.
Fonte: Boletim Científico – Março/22 (Greiner Bio-One)

por CenterLab | mar 3, 2022 | Informativos
Atualmente definida como uma síndrome adquirida, a coagulação intravascular disseminada (CIVD) é caracterizada pela ativação difusa da coagulação intravascular, levando à formação e deposição de fibrina na microvasculatura. Tal condição é associada às diversas entidades clínicas como trauma grave, tumores sólidos, neoplasias hematológicas, descolamento de placenta, embolia de líquido amniótico, hemangiomas gigantes, aneurismas de aorta, anemia hemolítica microangiopática, sobretudo infecções que levam à septicemia. Entretanto, numa hemostase normal o equilíbrio entre as proteínas pró-coagulantes e anticoagulantes é o que mantém a fluidez do sangue pelos vasos, incluindo o controle da hemorragia e dissolução de coágulos.
Com efeito, para manter esse equilíbrio existem 13 tipos diferentes de fatores de coagulação e os seus nomes são expressos em algarismos romanos (figura 1). Assim, existe desde o Fator I até o Fator XIII. Esses fatores são ativados, por exemplo, quando ocorre o rompimento do vaso sanguíneo, onde a ativação do primeiro leva à ativação do seguinte até que ocorra a formação do coágulo pela ação dos 13 fatores. A ativação descontrolada do sistema de coagulação não resulta apenas em trombose, mas também em inflamação e proliferação celular, mediadas principalmente pela ação da trombina. Desta forma, estabelece-se uma alça de retroalimentação positiva que se não controlada pode progredir promovendo lesão vascular, falência de múltiplos órgãos e morte.
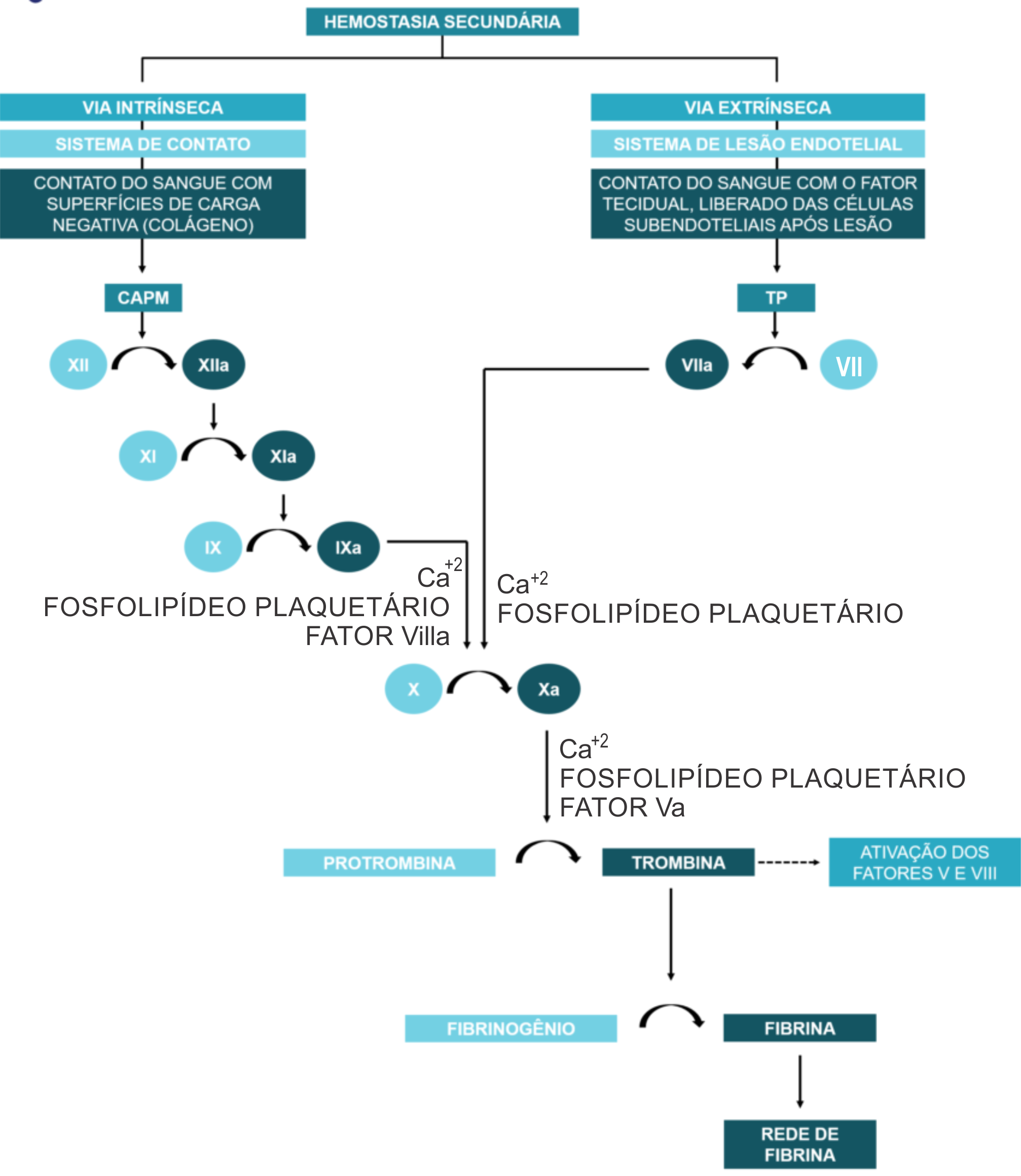
Figura 1: Esquema da cascata de coagulação com divisão do sistema em duas vias (intríseca e extrínseca).
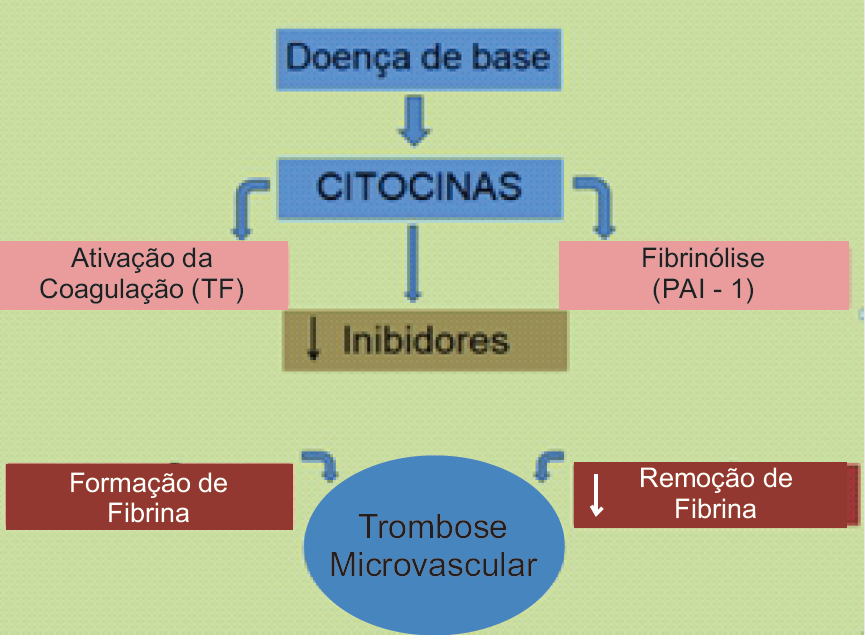
Diante da pandemia de coronavírus, diversos aspectos vêm sendo estudados na tentativa de conhecer melhor a doença e, dessa forma, reduzir o número e a gravidade dos indivíduos infectados. A literatura vigente descreve que a forma grave daCOVID-19 é frequentemente complicada com coagulopatia. Dentro desse contexto, a CIVD é relatada em grande parte dos óbitos. Em torno do 7º ao 12º dia dos sintomas transcorrem as complicações. A manifestação grave da infecção é marcada por uma resposta inflamatória imunológica acentuada, caracterizada pela presença de monócitos, linfócitos, neutrófilos e macrófagos. Em trabalhos já publicados, análises histológicas foram evidenciadas dano alveolar difuso, infiltrado inflamatório intersticial mononuclear com trombose em microcirculação e formação de membrana hialina. Essa resposta se dá pelo os altos índices de citocinas pró-inflamatórias no sistema circulatório, como IFN-γ, IL 1 e 6 e TNF-α, formando o conceito de tempestade de citocinas. Também, injúrias fora do âmbito do aparelho respiratório, bem como trombose podem acontecer sem que haja assiduidade local confirmada do vírus, admitindo que a infecção pelo SARS-CoV-2 compreenda uma severa resposta inflamatória, com estado de hipercoagulabilidade. Pacientes com infecção e que consequentemente desenvolvem resposta inflamatória sistêmica podem evoluírem com lesão
endotelial e consecutivo aumento na geração de trombina e diminuição da fibrinólise endógena. Pode-se assim denominar o estado pró-trombótico de Coagulopatia Induzida pela Sepse (SIC) que antecede a CIVD. A fisiologia que rege a SIC finaliza em uma condição próhemostática. Indivíduos que são acometidos por infecções virais estão sujeitos a evoluir para sepse associada à disfunção orgânica. A sepse está bem especificada como um dos fatores causais mais comuns da CIVD, que se desenvolve com a liberação de citocinas próinflamatórias, como fator de Von Willebrand e expressão do fator tecidual, que ativam monócitos e células endoteliais. A trombina circulante, não impedida pela via fisiológica anticoagulante, pode ativar as plaquetas e incitar a fibrinólise apontando para um estado hipercoagulável em pacientes diagnosticados com infecção, como na COVID-19. Ademais, o estado de hipóxia gerado na forma grave da patologia pode estimular a trombose, pelo aumento da viscosidade sanguínea e por uma via de sinalização dependente do fator de transcrição provocado por hipóxia. Estudos mostram relação cruzada entre inflamação e coagulação, sendo a inflamação responsável por provocar a ativação da coagulação. Contudo, fora do estado patológico, há um controle da ativação da coagulação por três vias anticoagulantes: sistema ativado da proteína C, inibidor da via do fator tecidual e o sistema antitrombina. No entanto, essas vias fisiológicas sofrem alterações na sepse.
Testes Laboratoriais de Coagulação
Não é de hoje que os testes laboratoriais possuem grande relevância no diagnóstico dos pacientes em diferentes situações clínicas. Sabe-se que, de um tempo para cá, os testes de hemostasia tornaram-se ponto crucial no processo, já que os seus números influenciam diretamente nas decisões clínicas. É fundamental para um diagnóstico e acompanhamento eficaz do paciente, que os diferentes processos da análise disponham de qualidade. Isso inclui o desempenho dos equipamentos laboratoriais e, principalmente, a qualidade dos reagentes utilizados para a realização dos exames. Logo, para monitorização de tratamentos com anticoagulantes.
Os testes deTP e TTPA são considerados testes de triagem da coagulação. É importante conhecer a sensibilidade destes testes na identificação da deficiência de diferentes fatores da coagulação. Um teste com pouca sensibilidade, ou seja, incapaz de identificar anormalidades pode gerar resultados inadequados que prejudicam a investigação das coagulopatias. A sensibilidade de um determinado reagente pode ser especifica para uso em um determinado equipamento ou para uso combinado com outros reagentes.
Tempo de Tromboplastina – TP
Os reagentes utilizados (tromboplastinas) inicialmente eram produzidos a partir de um tecido humano, e foram posteriormente sendo substituídos por reagentes de tecido animal, o que gerou enorme variação intra e interlaboratorial, ou seja, a sensibilidade dos reagentes variava de acordo com a origem da tromboplastina. Fato que ocasionou sérios problemas para os pacientes, visto que os resultados obtidos por laboratórios que utilizavam reagentes menos sensíveis, ocasionavam erroneamente em uso de doses mais altas de anticoagulantes. A origem da tromboplastina interfere na sua sensibilidade, por isso os resultados de um TP do mesmo paciente na mesma amostra podem variar de um laboratório para outro. Diante deste problema foi instituído pela Organização Mundial de Saúde (OMS) a RNI (Relação Normatizada Internacional), que expressa à uniformização dos resultados, pois leva em consideração a sensibilidade do reagente utilizado. Os fabricantes dos reagentes foram orientados a comparar as tromboplastinas produzidas com a tromboplastina de referência mundial da OMS, através da construção de uma curva de calibração, onde será verificada a atividade enzimática a partir da diluição seriada de um plasma calibrador, e calcular o Índice de Sensibilidade Internacional (ISI), diminuindo assim, as discrepâncias entre os resultados do tempo de protrombina, dando mais confiabilidade ao teste.
O TP é mais sensível á deficiência do fator VII e tem menor sensibilidade aos fatores da via comum e para deficiência de fibrinogênio. Atualmente, fator tecidual recombinante vem sendo cada vez mais utilizado, e o TP mensurado com essa tromboplastina parece ser mais confiável na identificação de variantes de deficiência de fator VII. Um exemplo de reagentes mundialmente reconhecidos por sua credibilidade e confiança são os da Instrumentation Laboratory®, integrante do grupo Werfen® desde 1991. Focado em inovação e melhorias constantes para testes de diagnóstico in vitro, o grupo Werfen® desenvolve, fabrica e distribui
reagentes da linha de hemostasia e dentre os principais testes da rotina de coagulação, pode-se elencar os reagentes de ponta desenvolvidos pelo fabricante, Recombiplastin2G, utilizado para a determinação quantitativa de TP – Tempo de Protrombina, que tem como grande diferencial a sua constituição ser derivado de fator tecidual humano através de tecnologia recombinante, O processo melhorado de produção utilizado para este reagente, assegura uma excelente uniformidade lote a lote e um desempenho superior em relação às tromboplastinas derivadas de fontes naturais. Devido a esta elevada sensibilidade a deficiência de fatores, comparável às Preparações Internacionais de Referência, é especialmente adequado para a monitorização da Terapêutica Anticoagulante Oral. Sua apresentação é liofilizada, de fácil reconstituição pelo operador e sua estabilidade após o preparo é excelente evitando o desperdício do reagente. Seu ISI (índice de padronização internacional) de 1,00 é um dos melhores valores encontrados no mercado. Além disso, o portifólio contempla com o TP-Fibrinogénio HS PLUS que é um extracto liofilizado de cérebro de coelho com uma concentração óptima de ions de cálcio. Devido a um processo de fabrico especial e meticuloso foi possível obter uma alta sensibilidade em relação aos factores II, V, VII e X, dando resultados comparáveis com o Padrão de Referência Internacional. A alta sensibilidade analítica faz com que este reagente seja particularmente apropiado também para a monitorização da terapêutica anticoagulante.
Tempo de Tromboplastina Parcial Ativada – TTPa
O reagente mais moderno e utilizado em grandes centros laboratoriais é o HemosiL APTT-SP. Este é derivado de tecnologia de fosfolipídios sintéticos, contendo como ativador as partículas de sílica micronizada. Essa tecnologia garante uma maior reprodutibilidade, estabilidade e sensibilidade frente a outros reagentes de TTPa, dentre eles, o HemosiL SynthASil e o HemosiL SynthAFax, proporcionando resultados mais precisos perante o déficit de Factor XII, XI, X, IX, VIII, V, II, ou Fibrinogénio, doenças hepáticas, défice de Vitamina K, presença de heparina, anticoagulante lúpico ou outros inibidores. Possui apresentação líquida e pronta para uso, o que também impacta positivamente no resultado dos testes.
D-Dímero
Atualmente, outro ensaio que tem se destacado no mercado é o teste de D-dímero que é utilizado para avaliação de pacientes com COVID 19. A IL possui diferentes apresentações deste insumo, para atender a necessidade de cada laboratório. As duas mais conhecidas e aplicadas são: D-dimer 500 e D-dimer HS500. A diferença entre eles é o modo de preparo, já que um está pronto para uso e o outro necessita ser reconstituído. Ambos os kits são para a determinação quantitativa do D-dímero no plasma humano, com uma ótima linearidade e sensibilidade, cut-off validado de 500ng/mL e resultados liberados em menos de 5 minutos nos sistemas IL.
Com 40 anos dedicados ao mercado de diagnósticos laboratoriais, a Centerlab® em parceria com o grupo Werfen® oferecem as linhas de reagentes de hemostasia, Hemosil Recombiplastin2G e APTT-SP, além dos sistemas ACL ELITE PRO Family e ACL TOP Family Série 50 com gerenciamento de automação e qualidade mais avançado em testes de hemostase. Ideal para testes de hemostasia de rotina e especialidade, incluindo ensaios de coagulação, cromogênicos e imunológicos em laboratórios clínicos de médio a alto volume.
Referências:
-https://newslab.com.br/a-j-r-ehlke-em-parceria-com-a-werfen-aposta-na-tecnologia-de-ponta-a-favor-da-confiabilidade-no-diagnostico-em-hemostasia/
– https://www.centerlab.com/blog/Centernews_107/
– https://bvsms.saude.gov.br/bvs/publicacoes/manual_diagnostico_laboratorial_coagulopatias_plaquetopatias.pdf
– http://editora.universidadedevassouras.edu.br/index.php/RS/article/view/2330
– https://editoraime.com.br/revistas/index.php/rems/article/view/623
Página 3 de 30«12345...102030...»Última »