por CenterLab | jan 28, 2020 | Informativos
Fêmea do Aedes aegypti é responsável pela transmissão da febre amarela, dengue, chikungunya e zika vírus — Foto: Pixabay/Divulgação
Todo o Nordeste, assim como Espírito Santo e Rio de Janeiro, estão sendo monitorados, afirmou o porta-voz da pasta ao G1. O surto é esperado a partir de março.
Os estados do Nordeste, assim como Espírito Santo e Rio de Janeiro, poderão ter um surto de dengue a partir de março de 2020, afirma o Ministério da Saúde.
“A dengue é uma doença sazonal e o quadro é dinâmico e pode mudar em pouco tempo, mas, no momento, os nove estados do Nordeste e as regiões do Sudeste com grande contingente populacional pouco afetadas em 2019 estão no nosso alerta”, afirmou ao G1 coordenador-geral de vigilância em arbovirose do Ministério da Saúde, Rodrigo Said.
O Brasil registrou 1.544.987 casos de dengue no ano passado, com 782 mortes, segundo dados da pasta, um aumento de 488% em relação a 2018, um ano considerado atípico pelo Ministério.
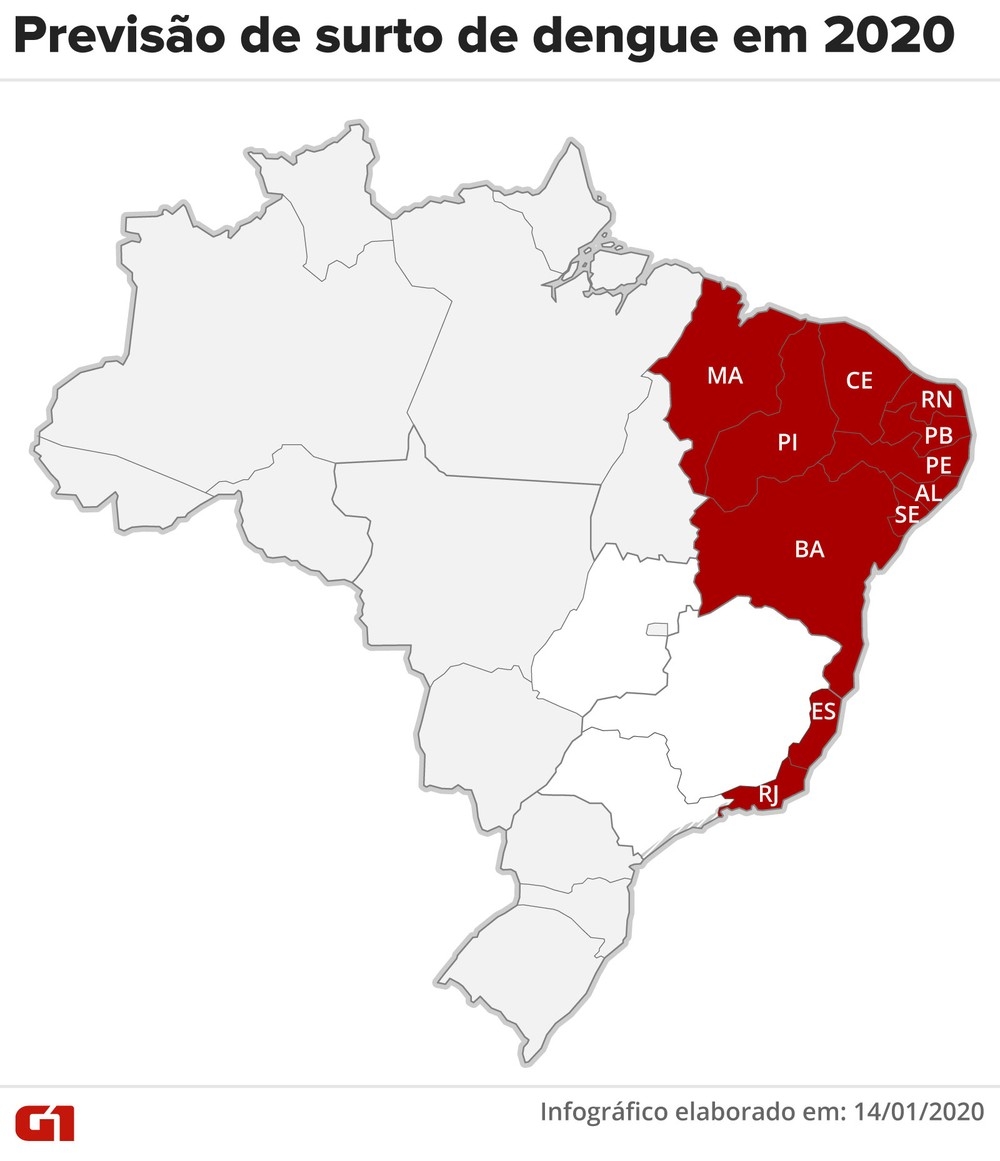
Mapa mostra estados do país que poderão ter surto de dengue em 2020 — Foto: Fernanda Garrafiel/G1
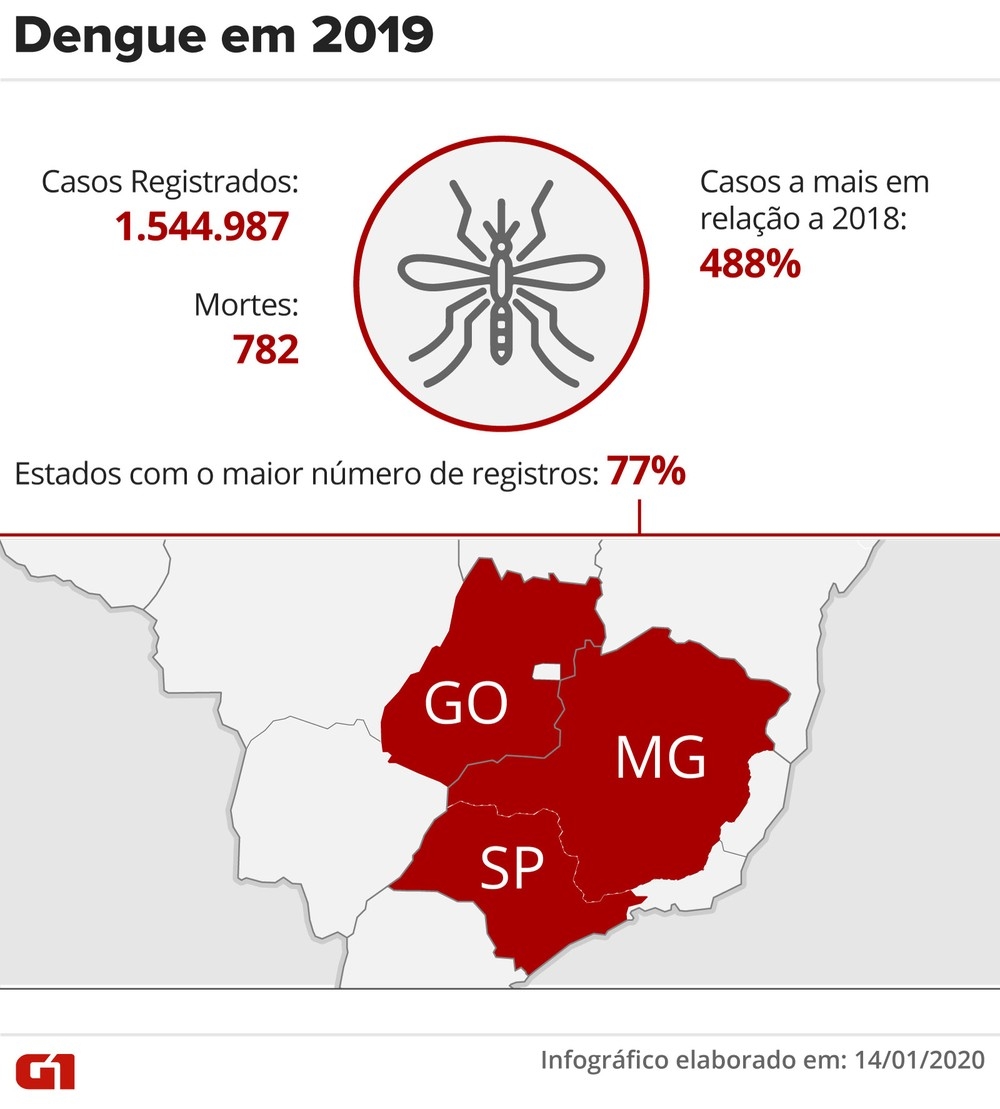
Infográfico mostra os casos registrados de dengue e estados com maior número de registros — Foto: Fernanda Garrafiel/G1
Variações de ano a ano
Segundo Said, 2017 e 2018 foram anos com poucos casos de dengue quando comparados a 2015 e 2016.
“Isso aconteceu porque circulou, em todos esses anos, o mesmo sorotipo do vírus da dengue. E quando uma pessoa é infectada pela dengue, ela estará imune aquele determinado sorotipo pra sempre, mas não aos outros sorotipos da doença”, afirma.
A dengue é transmitida por quatro sorotipos do vírus: o sorotipo 1, 2, 3 e 4, todos em circulação no Brasil.
A intensidade de circulação desses sorotipos se alterna pelo país de tempos em tempos. Os surtos de dengue costumam ocorrer, segundo Said, quando há mudança na circulação do tipo de vírus.
Foi o que ocorreu no final de 2018, quando começou a circular no Sudeste e Centro-Oeste um tipo diferente dos anos anteriores, o sorotipo 2. “As pessoas não estavam imunes ao sorotipo 2, que não circulava no país desde 2008. Por isso ele veio tão forte, porque encontrou novas pessoas para infectar”, explica o porta-voz.
A recente circulação do sorotipo 2 aconteceu somente em algumas partes do Sudeste e Centro-Oeste, o que ajuda a entender porque 77% de todos os registros de dengue no país, assim como 67% das mortes, ocorreram em apenas três estados em 2019: São Paulo, Minas Gerais e Goiás.
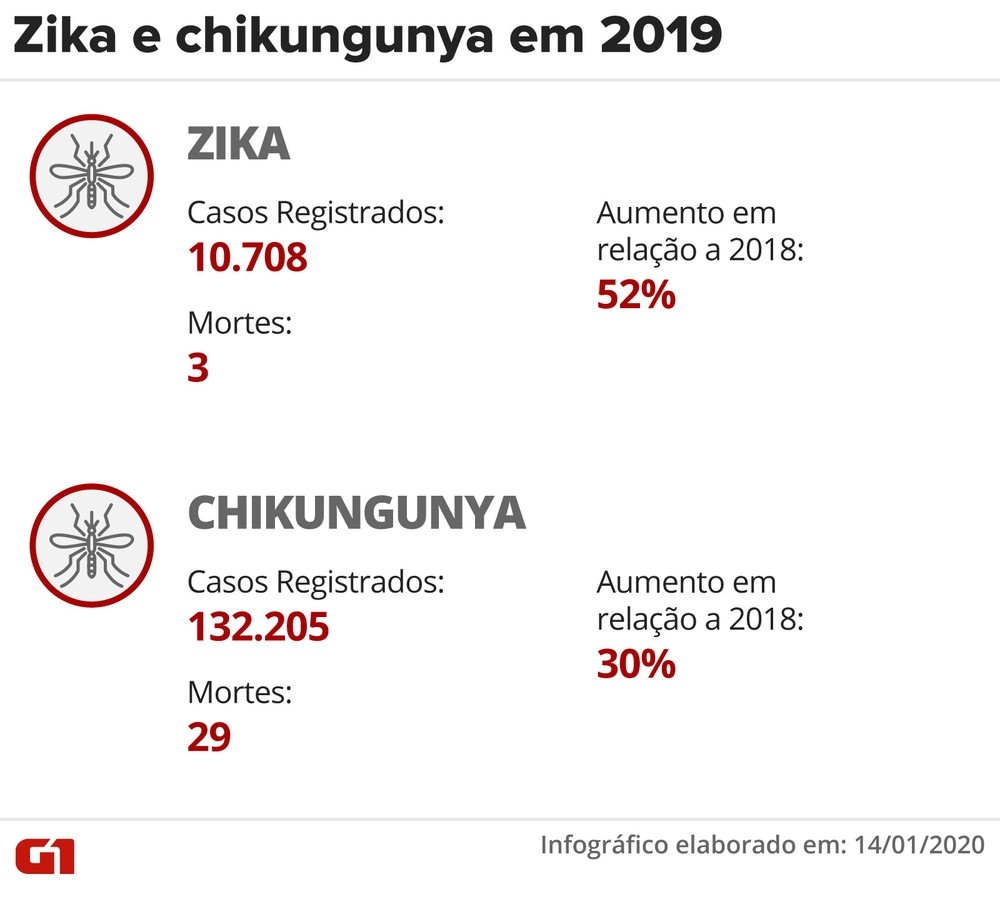
Infográfico mostra número de casos de Zika e Chikungunya em 2019 — Foto: Fernanda Garrafiel/G1
Fonte:
G1
por CenterLab | jan 27, 2020 | Informativos
Com a chegada do verão, as temperaturas se elevam e o uso de aparelhos de ar condicionado é inevitável.
O problema é que, apesar do conforto térmico oferecido pelo aparelho, estamos expostos à ação nociva da bactéria Legionella.
O gênero Legionella tem sido reconhecido como importante agente etiológico causador da doença do trato respiratório, a Legionelose ou Doença do Legionário, conhecida assim após a Convenção da Legião Americana em 1976, na Filadélfia, onde 34 participantes morreram e 221 adoeceram com pneumonia.
A doença do Legionário se caracteriza por pneumonia aguda com febre alta, dores de cabeça, calafrios, diarreia e tosse seca, mas pode resultar em graves complicações, incluindo a morte em situações extremas. Uma vez que a Legionella pneumophila é aspirada, ela se aloja nos alvéolos pulmonares e pode causar uma forte pneumonia.
Legionella é uma bactéria aquática e tem sido isolada em sistemas de ar condicionado, que apresentam condições favoráveis para proliferação. A presença desses organismos em sistemas de ar configura um problema de Saúde Pública, pois essas bactérias podem ser inaladas juntamente com partículas suspensas de poeira ou aerossóis originários dos sistemas de ar condicionado.
Existem 50 espécies e 70 serogrupos distintos. Pelo menos 20 espécies de Legionella estão associadas a doenças no ser humano, a Legionella pneumophila (16 serogrupos) é responsável por 70 a 90 % das infecções no homem.
No Brasil, existem diversos estudos sobre o assunto. Um estudo avaliou a ocorrência do gênero Legionella em amostras de água de residências, edifícios públicos, hospitais e plantas industriais em São Paulo e encontraram que, das 69 amostras analisadas, 6 foram positivas para a presença de Legionella sp.
Outro estudo, analisou amostras de água de cinco hospitais no Rio de Janeiro. O resultado revelou a presença de Legionella pneumophila sorogrupo 1 em todas as amostras examinadas.
Um estudo analisou 67 amostras de água de reservatórios naturais, torres de resfriamento, clínicas dentárias, sistemas de aquecimento e condensadores na cidade de São Paulo e encontrou o gênero Legionella em 9 amostras.
Esses resultados denotam que a manutenção preventiva desses equipamentos merece especial atenção. A presença dessa bactéria representa risco aos ocupantes de ambientes climatizados, especialmente no ambiente hospitalar.
Fonte: Eco Diagnóstica
por CenterLab | jan 27, 2020 | Informativos
Foto: Site Kasvi
Muitas doenças comuns no Brasil e no mundo deixaram de ser um problema de saúde pública por causa da vacinação massiva da população. Poliomielite, rubéola, tétano e coqueluche são só alguns exemplos de doenças comuns no passado e que as novas gerações só ouvem falar em histórias. No entanto, se a população parar de vacinar seus filhos, algumas doenças que já são erradicadas podem voltar a aparecer e causar novas epidemias, como os recentes casos de sarampo.
COMO FUNCIONAM AS VACINAS
O objetivo das imunizações é estimular o nosso organismo a produzir anticorpos contra determinados patógenos, principalmente bactérias e vírus, mas sem o desenvolvimento da doença.
Quando uma pessoa é infectada pela primeira vez por um antígeno, o sistema imunológico produz anticorpos para combater o invasor. No entanto, a produção não é feita numa velocidade suficiente para prevenir a doença, já que o sistema imunológico não conhece aquele invasor, provocando assim, o desenvolvimento da doença. Se aquele organismo invadir o corpo novamente, o sistema imunológico vai produzir anticorpos em uma velocidade suficiente para evitar que a pessoa fique doente uma segunda vez. Essa proteção é chamada de imunidade.
Com os mesmos antígenos que causam uma doença, mas enfraquecidos ou mortos, a vacina ensina e estimula o sistema imunológico a produzir os anticorpos que levam a imunidade. Assim, se você for exposto a esse organismo, as células da memória (linfócitos B) adormecidas do seu sistema imunológico o reconhecerão imediatamente e rapidamente começarão a se multiplicar e produzir os anticorpos. Essa resposta imune acelerada e mais intensa é conhecida como resposta secundária. É mais rápido e mais eficaz, porque todos os “preparativos” para o ataque foram feitos quando você foi vacinado.
É NORMAL TER FEBRE
A sensação de mal-estar que pode surgir depois da imunização é comum, e até mesmo esperada pelos médicos e especialistas porque quando o antígeno é injetado, o corpo vai gerar uma reação a esse corpo estranho. O organismo identifica o corpo estranho e produz anticorpos, gerando uma reação inflamatória. É essa reação inflamatória do corpo que pode produzir a febre, o mal-estar e a dor no local, pois mostra a reação do organismo.
TIPOS DE VACINAS
Existem 4 tipos principais de vacinas:
– VACINAS VIVAS ATENUADAS
Contêm uma forma viva, mas enfraquecida, do organismo. Ou seja, fracos o suficiente para não conseguirem causar sintomas relevantes. Costumam ser os melhores estimulantes para a produção de anticorpos pelo sistema imune. Este tipo de vacina costuma requerer apenas uma ou duas doses e produz uma imunização por muitos anos, às vezes para o resto da vida.
Ex: BCG, catapora, rubéola, caxumba, varíola, sarampo, febre amarela.
– Vacinas inativadas
Contêm uma forma morta do organismo. Por isso costumam apresentar uma capacidade de imunização mais baixa, sendo necessárias mais de uma dose para criar uma proteção prolongada. Em alguns casos a imunização desaparece após alguns anos, sendo necessária a aplicação de doses de reforço.
Ex: Pólio, cólera, raiva, influenza (gripe), tifo, hepatite A.
– Vacinas de subunidades
Contêm apenas a parte do organismo que estimula uma resposta imune.
Ex: Hepatite B, meningite, pneumococo, HPV, Haemophilus influenzae.
– Vacinas contra toxoides
Contêm uma toxina bacteriana inativada (toxóide). Os toxoides também costuma gerar uma imunização fraca, desse modo, é necessário reforço após alguns anos.
Ex: Tétano, difteria.
DOENÇAS NÃO DESAPARECEM
Sabemos que uma doença que aparentemente está sob controle pode voltar repentinamente, porque infelizmente, já vimos isso acontecer.
Quando uma alta proporção da população está vacinada, o resultado é a prevenção da disseminação da doença – algo que, por consequência, dá proteção às pessoas que não desenvolveram imunidade ou que não podem ser vacinadas. Isso é chamado de imunidade de rebanho. Quando ela deixa de existir, surge um risco de contaminação à população como um todo.
A varíola é a única doença que foi totalmente apagada do planeta
Casos recentes de sarampo – doença que era considerada erradicada do Brasil desde 2016 – que registraram quase 13,5 mil casos confirmados e 15 mortes no país em 2019, apenas reforçam a importância da imunização.
Essas consequências são decorrentes dos baixos índices de vacinação no Brasil. Nos últimos anos, a meta de cobertura populacional foi de 95%, entretanto, segundo a OMS, na maioria dos estados brasileiros, não se atingiu nem 75% da população.
A proporção de uma população que precisa ser vacinada para que seja mantida a imunidade de rebanho varia conforme a doença, para sarampo, por ser altamente contagiosa, é de 95%.
MOVIMENTO ANTIVACINA
O movimento antivacina surgiu em 1998 em Londres pouco tempo depois da publicação de um estudo feito por Andrew Wakefield, então lançado em uma revista científica que relacionava a vacina triplex – utilizada contra rubéola, caxumba e sarampo – ao autismo. No entanto, pouco tempo depois, diversos outros estudos foram publicados desmentindo a teoria.
Em 2004, o Instituto de Medicina dos EUA concluiu que não havia provas de que o autismo tivesse relação com os componentes da vacina. Em seguida, no mesmo ano, descobriu-se que, antes da publicação de seu estudo, Wakefield havia feito um pedido de patente para uma vacina contra sarampo que concorreria com a MMR, algo que foi visto como um conflito de interesses.
Além disso, um assistente de Wakefield afirmou que, em seu estudo, o médico manipulou informações de crianças para forçar a ligação entre a vacina e o autismo. Desse modo, em 2010, o Conselho Geral de Medicina do Reino Unido julgou Wakefield “inapto para o exercício da profissão”, qualificando seu comportamento como “irresponsável”, “antiético” e “enganoso”. Logo após, a Lancet, periódico que havia tornado público seu estudo, se retratou da publicação, dizendo que suas conclusões eram “totalmente falsas”.
A Organização Mundial da Saúde (OMS) considera a questão dos movimentos antivacina tão preocupante, que a listou como uma das dez maiores ameaças à saúde global em 2019.
Foto: Kasvi
por CenterLab | jan 27, 2020 | Informativos
O teste tempo de sangramento (TS) deixou de fazer parte do coagulograma na rotina do Fleury
Publicado em 17 de julho de 2019
Desde o começo de fevereiro de 2018, o Fleury deixou de realizar o teste tempo de sangramento (TS) como parte do coagulograma. Contudo, o conjunto de exames para avaliação da coagulação foi mantido no portfólio, o que inclui a contagem de plaquetas, o tempo de protrombina e o tempo de tromboplastina parcial ativada.
Originalmente introduzido como uma ferramenta para avaliação da função plaquetária, o TS parou de ser feito em inúmeros países, a exemplo dos Estados Unidos, devido a dificuldades associadas à sua padronização, à sua baixa sensibilidade e especificidade, a interferências relacionadas à habilidade do técnico que o executa e à pouca reprodutibilidade do teste, de forma que seus resultados não expressam, necessariamente, o risco hemorrágico do indivíduo. Ademais, condições inerentes ao próprio paciente, como redução do número de plaquetas funcionalmente ativas e uso de medicamentos, podem interferir na função plaquetária.
Causas: Doenças do colágeno.
Comentários: Síndrome de Ehlers Dantos.
Causas: Trombocitopenias.
Comentários: Contagens plaquetárias inferiores a 50.000/mm³ podem interferir no resultado do teste.
Causas: Trombopatias.
Comentários: Trombopatias congênitas e algumas condições adquiridas, como paraproteinemias, uremia, doenças mieloproliferativas e síndrome mielodisplásica, podem causar defeitos na função plaquetária e prolongar o TS.
Causas: Doença de von Willebrand (DVW).
Comentários: Na DVW, o TS pode ou não estar prolongado. Dessa forma, o teste não é mais recomendado para diagnóstico.
Causas: Anemia grave.
Comentários: Pacientes com anemia apresentam mudanças na distribuição das plaquetas e, portanto, menor interação dessas células com o endotélio.
Causas: Hipofibrinogenemia.
Comentários: O fibrinogênio é essencial para que ocorra a agregação plaquetária e, portanto, indivíduos com deficiência desse fator apresentam prolongamento do TS.
Causas: Medicamentos.
Comentários: Clopidogrel, ácido acetilsalicílico e outros anti-inflamatórios não esteroidais podem prolongar o TS. Entretanto, o teste não é capaz de predizer o risco de sangramento perioperatório de pacientes em uso dessas medicações.
Uma vez que não existe um exame para substituir o TS na avaliação pré-cirúrgica do risco hemorrágico, a investigação adicional do paciente deve ser direcionada pela história pessoal e familiar de sangramento, podendo contemplar desde testes de agregação plaquetária, quando há suspeita de plaquetopenias hereditárias, até métodos que avaliam a função das plaquetas, como o PFA-100, na hipótese de alteração medicamentosa ou de doença de von Willebrand.
Fonte: Fleury
por CenterLab | jan 13, 2020 | Informativos
De acordo com a Organização Mundial da Saúde (OMS) são contabilizados todos os dias no mundo mais de 1 milhão de casos de IST curáveis entre pessoas de 15 a 49 anos.
As IST estão em alta no Brasil e a sífilis é o caso mais alarmante com aumento da taxa de 59.1 casos/100 mil habitantes em 2017 para 75.8 casos/100 mil habitantes em 2018.
As hepatites virais, doenças altamente perigosas, também estão em alta. De 2008 até 2018 foram registrados quase 633 mil casos no país, sendo que somente em 2018 foram 43 mil casos.
Para HIV, de 2010 a 2018 o Brasil teve aumento de 21% no número de casos novos, enquanto o resto do planeta teve queda de 16%.
De acordo com especialista, a principal razão para esse aumento está ligada ao fato das doenças serem silenciosas e não apresentarem sinais e sintomas por meses ou anos, somado a diminuição no uso de preservativos, o baixo nível de conhecimento sobre educação sexual e baixa adesão na cobertura vacinal para as doenças que podem ser prevenidas.
As IST são causadas por mais de 30 vírus e bactérias e transmitidas, principalmente, por relação sexual com uma pessoa infectada. Também podem ser passadas de mãe para criança durante gestação, parto ou amamentação. Essas doenças podem provocar, além das conhecidas lesões nos órgãos genitais, câncer, complicações na gravidez e no pato, aborto, infertilidade, problemas neurológicos, cardiovasculares e até a morte. Podem, também, deixar sequelas emocionais e sociais.
Outro fator preocupante é que essas doenças deixam os pacientes mais vulneráveis a adquirir o HIV. Exima-se que a chance de infecção eleva em até 18 vezes.
Fonte: Eco Diagnóstica